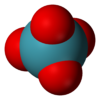
செனான் நான்காக்சைடு
செனான் நான்காக்சைடு (Xenon tetroxide) என்பது XeO4 என்ற மூலக்கூற்று வாய்ப்பாடு கொண்ட கனிம வேதியியல் சேர்மமாகும். செனான் மற்றும் ஆக்சிசன் சேர்ந்து உருவாகும் இச்சேர்மம் மந்த வாயுச் சேர்மங்களில் நிலைப்புத்தன்மை கொண்ட சேர்மமாக காணப்படுகிறது. மஞ்சள் நிறத்தில் படிகவடிவத் திண்மமான இச்சேர்மம் −35.9 °செ வெப்பநிலைக்கு கீழ் நிலைப்புத் தன்மையுடன் காணப்படுகிறது. இவ்வெப்பநிலைக்கு மேல் இது தலைகீழாக வெடிக்கும் தன்மை கொண்டு சிதைவடைந்து தனிமநிலை செனான் மற்றும் ஆக்சிசனாக மாறுகிறது.[4][5]
| |||
| பெயர்கள் | |||
|---|---|---|---|
| ஐயூபிஏசி பெயர்s
செனான் டெட்ராக்சைடு
செனான்(VIII) ஆக்சைடு | |||
| வேறு பெயர்கள்
செனான் நான்காக்சைடு
பெர்செனிக் நீரிலி | |||
| இனங்காட்டிகள் | |||
| 12340-14-6 | |||
| ChemSpider | 21106492 | ||
| யேமல் -3D படிமங்கள் | Image | ||
SMILES
| |||
| பண்புகள் | |||
| XeO4 | |||
| வாய்ப்பாட்டு எடை | 195.29 கி மோல்−1 | ||
| தோற்றம் | மஞ்சள் திண்மம்−36°செ கீழ் | ||
| அடர்த்தி | ? கி.செ.மீ−3, திண்மம் | ||
| உருகுநிலை | −35.9 °C (−32.6 °F; 237.2 K) | ||
| கொதிநிலை | 0 °C (32 °F; 273 K) [1] | ||
| கட்டமைப்பு | |||
| மூலக்கூறு வடிவம் | |||
| இருமுனைத் திருப்புமை (Dipole moment) | 0 D | ||
| வெப்பவேதியியல் | |||
| Std enthalpy of formation ΔfH |
+153.5 கி.கலோரி மோல் −1 [3] | ||
| நியம மோலார் எந்திரோப்பி S |
? J.K−1.mol−1 | ||
| தீங்குகள் | |||
| ஈயூ வகைப்பாடு | வெடிக்கும் (E) | ||
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |||
| | |||
| Infobox references | |||
செனானின் எட்டு இணைதிறன் எலக்ட்ரான்களும் ஆக்சிசனுடன் பிணைப்பில் பங்கு கொள்கின்றன. இச்சேர்மத்தில் செனானின் ஆக்சிசனேற்ற நிலை +8. ஆகும். ஆக்சிசன் மட்டுமே செனானை அதனுடைய அதிகபட்ச ஆக்சிசனேற்ற நிலையில் வினையில் ஈடுபடுத்துகிறது. புளோரினும் கூட XeF6 என்ற சேர்மமாக (+6) ஆக்சிசனேற்ற நிலையைத் தரமுடிகிறது. செனான் நான்காக்சைடு மற்றும் செனான் அறுபுளோரைடு ஆகியன வினை புரிவதால் XeO3F2 மற்றும் XeO2F4 என்ற ஆக்சிசனேற்ற நிலை +8, கொண்ட சேர்மங்கள் தயாரிக்கப்படுகின்றன. இவை குறுகிய வாழ்நாள் கொண்ட சேர்மங்களாகும். அடர்த்திவழி பிரிகை முறையில் XeO3F2 மற்றும் XeO2F4 சேர்மங்களை கண்டறிய இயலும். பெர்செனேட்டு சேர்மங்களிலும் செனான் +8 ஆக்சிசனேற்ற நிலையில் காணப்படுகிறது.
வினைகள் தொகு
இச்சேர்மம் −35.9 °செ வெப்பநிலைக்கு வெடிக்கும் தன்மையுடன் காணப்படுகிறது. இதனால் சிதைவடைந்து செனான் மற்றும் ஆக்சிசன் வாயுக்களாக (ΔH = −643 கியூ/மோல்) சிதைவடைகிறது.
- XeO4 → Xe + 2 O2
தண்ணீரில் செனான் நான்காக்சைடு கரைந்து பெர்செனிக் அமிலமாகவும் காரத்தில் கரைந்து பெர்செனேட்டு உப்புகளாக்வும் உருவாகிறது.
- XeO4 + 2 H2O → H4XeO6
- XeO4 + 4 NaOH → Na4XeO6 + 2 H2O
செனான் நான்காக்சைடு , செனான் அறுபுளோரைடுடனும் வினைபுரிந்து செனான் ஆக்சிபுளோரைடுகளைக் கொடுக்கிறது.
XeO4 + XeF6 → XeOF4 + XeO3F2 XeO4 + XeF6 → XeO2F4 + XeO2F2
தொகுப்பு வினைகள் தொகு
அனைத்து தொகுப்பு வினைகளும் பெர்செனேட்டுகளில் இருந்து தொடங்குகின்றன. இவை செனேட்டுகளில் இருந்து இரண்டு முறைகளில் பெறப்படுகின்றன. செனேட்டுகள் விகிதச்சமமாதலின்றி பிரிகையடைந்து செனேட்டுகள் மற்றும் பெர்செனேட்டுகளாக பிரிகைய்டையும் முறை முதலாவது முறையாகும்.
- 2 HXeO4− + 2 OH− → XeO64− + Xe + O2 + 2 H2O
இரண்டாவது முறை காரக் கரைசலில் செனேட்டுகளை ஓசோனுடன் சேர்த்து ஆக்சிசனேற்றம் செய்யும் முறையாகும்.
- HXeO4− + O3 + 3 OH− → XeO64− + O2 + 2 H2O
பேரியம் பெர்செனேட்டு கந்தக அமிலத்துடன் வினைபுரிந்து நிலைப்புத்தன்மையற்ற பெர்செனிக் அமிலம் உருவாகி பின்னர் இது நீர்நீக்கமடைந்து செனான் நான்காக்சைடு உருவாகிறது.:[6]
- Ba
2XeO
6 + 2 H
2SO
4 → 2 BaSO
4 + H
4XeO
6 - H
4XeO
6 → 2 H
2O + XeO
4
அதிகமாக எஞ்சியிருக்கும் பெர்செனிக் அமிலம் சிதைவடைந்து செனிக் அமிலமாக்வும் ஆக்சிசனாகவும் சிதைவடைகிறது.
- 2 H
4XeO
6 → O
2 + 2 H
2XeO
4 + 2 H
2O
மேற்கோள்கள் தொகு
- ↑ Lide, David R. (1998). Handbook of Chemistry and Physics (87 ). Boca Raton, FL: CRC Press. பக். 494. பன்னாட்டுத் தரப்புத்தக எண்:0-8493-0594-2. https://archive.org/details/isbn_9780849305948
- ↑ G. Gundersen, K. Hedberg, J. L.Huston (1970). "Molecular Structure of Xenon Tetroxide, XeO4". J. Chem. Phys. 52 (2): 812–815. doi:10.1063/1.1673060.
- ↑ Gunn, S. R. (May 1965). "The Heat of Formation of Xenon Tetroxide". Journal of the American Chemical Society 87 (10): 2290–2291. doi:10.1021/ja01088a038.
- ↑ H.Selig , J. G. Malm , H. H. Claassen , C. L. Chernick , J. L. Huston (1964). "Xenon tetroxide -Preparation + Some Properties". Science 143 (3612): 1322–3. doi:10.1126/science.143.3612.1322. பப்மெட்:17799234.
- ↑ J. L. Huston, M. H. Studier, E.N. Sloth (1964). "Xenon tetroxide - Mass Spectrum". Science 143 (3611): 1162–3. doi:10.1126/science.143.3611.1161-a. பப்மெட்:17833897.
- ↑ A. Earnshaw; Norman Greenwood (1997). Chemistry of the Elements (2nd ). Elsevier. பக். 901. பன்னாட்டுத் தரப்புத்தக எண்:9780080501093.