4-தொலுயீன்சல்போனைல் குளோரைடு
4-தொலுயீன்சல்போனைல் குளோரைடு (4-Toluenesulfonyl chloride) என்பது C7H7ClO2S என்ற மூலக்கூற்று வாய்ப்பாடு கொண்ட ஒரு கரிமச் சேர்மமாகும். CH3C6H4SO2Cl என்ற கட்டமைப்பு வாய்பாட்டாலும் இதை அடையாளப்படுத்தலாம். பாரா-தொலுயீன்சல்போனைல் குளோரைடு, தொலுயீன்-பாரா-சல்போனைல் குளோரைடு என்ற பெயர்களாலும் இச்சேர்மம் அழைக்கப்படுகிறது. வெள்ளை நிறத்தில் துர்நாற்றம் வீசும் திண்மப் பொருளாக 4-தொலுயீன்சல்போனைல் குளோரைடு காணப்படுகிறது. கரிமத் தொகுப்பு வினைகளில் பரவலாக ஒரு வினையாக்கியாகப் பயன்படுத்தப்படுகிறது.[2] தொலுயீனின் வழிப்பெறுதியான இச்சேர்மத்தில் சல்போனைல் குளோரைடு (−SO2Cl) என்ற வேதி வினைக்குழு இணைக்கப்பட்டிருக்கும்.
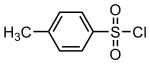
| |
| |
| பெயர்கள் | |
|---|---|
| விருப்பத்தெரிவு ஐயூபிஏசி பெயர்
4-மெத்தில்பென்சீன்-1-சல்போனைல் குளோரைடு | |
| வேறு பெயர்கள்
தோசில் குளோரைடு, பாரா-தொலுயீன்சல்போனைல் குளோரைடு,
| |
| இனங்காட்டிகள் | |
| 98-59-9 | |
| ChemSpider | 7119 |
| யேமல் -3D படிமங்கள் | Image |
| பப்கெம் | 7397 |
| |
| UNII | 027KYN78B4 |
| பண்புகள் | |
| C7H7ClO2S | |
| வாய்ப்பாட்டு எடை | 190.65 கி/மோல் |
| தோற்றம் | வெண் திண்மம் |
| உருகுநிலை | 65 முதல் 69 °C (149 முதல் 156 °F; 338 முதல் 342 K) |
| கொதிநிலை | 134 °C (273 °F; 407 K) at 10 மி.மீ.பாதரசம் |
| நீருடன் வினை புரியும் | |
| தீங்குகள் | |
| முதன்மையான தீநிகழ்தகவுகள் | Releases HCl on contact with water |
| தீப்பற்றும் வெப்பநிலை | 128 °C (262 °F; 401 K) |
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |
பயன்கள்
தொகுசிறப்பியல்பு முறையில், 4-தொலுயீன்சல்போனைல் குளோரைடு ஆல்ககால்களை (சுருக்கமாக ROH) தொடர்புடைய தொலுயீன்சல்போனேட்டு எசுத்தர்களாக அல்லது தோசில் வழிப்பெறுதிகளாக (தோசிலேட்டுகள்) மாற்றுகிறது:
- CH3C6H4SO2Cl + ROH → CH3C6H4SO2OR + HCl
இலித்தியம் அலுமினியம் ஐதரைடைப் பயன்படுத்தி தோசிலேட்டுகளை சிதைக்க முடியும்.
- 4 CH3C6H4SO2OR + LiAlH4 → LiAl(O3SC6H4CH3)4 + 4 RH
இவ்வாறான தோசிலேற்றமும் குறைப்பும் ஐதராக்சில் குழுவை அகற்ற அனுமதிக்கின்றன.
இதுபோலவே அமீன்களிலிருந்து சல்போனமைடைத் தயாரிக்கவும் 4-தொலுயீன்சல்போனைல் குளோரைடு பயன்படுத்தப்படுகிறது:[3]
- CH3C6H4SO2Cl + R2NH → CH3C6H4SO2NR2 + HCl
இதன் விளைவாக உருவாகும் சல்போனமைடுகள் காரத் தன்மை அல்லாதவையாகும். முதன்மை அமின்களிலிருந்து பெறப்பட்டாலும் கூட இவை அமிலத்தன்மையும் அற்றவையாகும்.
4-தொலுயீன்சல்போனைல் குளோரைடு ஐதசீனுடன் வினை புரிந்து பாரா-தொலுயீன் சல்போனிக் ஐதரசைடைக் கொடுக்கிறது.
தோசில் எசுத்தர்கள் மற்றும் அமைடுகளின் தயாரிப்பு ஒரு காரத்தின் முன்னிலையில் நடத்தப்படுகிறது. இது ஐதரசன் குளோரைடை உறிஞ்சுகிறது. தோசிலேற்ற செயல்முறைக்கு காரத்தின் தேர்வு பெரும்பாலும் முக்கியமானது. வழக்கமான காரங்களாக பிரிடின் மற்றும் டிரையெத்திலமீன் ஆகியவை அடங்கும். அசாதாரண காரங்களும் இவ்வினைக்குப் பயன்படுத்தப்படுகின்றன; எடுத்துக்காட்டாக, மும்மெத்திலமீன் முன்னிலையில் வினையூக்க அளவுக்கு மும்மெத்திலமோனியம் குளோரைடு மிகவும் பயனுள்ளதாக இருக்கும்.[2]
பிற வினைகள்
தொகுபரவலாகக் கிடைக்கக்கூடிய வினைப்பொருளாக இருப்பதால், வினைத்திறனின் கண்ணோட்டத்தில் 4-தொலுயீன்சல்போனைல் குளோரைடு பெரிதும் ஆராயப்பட்டது. நைட்ரைல்கள், ஐசோசயனைடுகள் மற்றும் ஈரிமைடுகளை உருவாக்க நீர் நீக்க வினைகளில் இது பயன்படுத்தப்படுகிறது. கந்தக மையத்தை நோக்கமாகக் கொண்ட ஒர் அசாதாரண வினையில், துத்தநாகம் 4-தொலுயீன்சல்போனைல் குளோரைடை சல்பினேட்டாகக் (CH3C6H4SO2Na ஆகக் குறைக்கிறது.[4]
பெருமளவு தயாரிப்பு
தொகுஇந்த வினையாக்கி ஆய்வகப் பயன்பாட்டிற்கு மலிவாக கிடைக்கிறது. உணவுசேர் பொருள்கள் தயாரிப்பதற்கான முன்னோடியான ஆர்த்தோ-தொலுயீன்சல்போனைல் குளோரைடை தொலுயீன் குளோரோசல்போனேற்றம் மூலம் உற்பத்தி செய்யும் போது இது ஒரு துணை தயாரிப்பு ஆகும்: :[5]
- CH3C6H5 + SO2Cl2 → CH3C6H4SO2Cl + HCl
4-தொலுயீன்சல்போனைல் குளோரைடு அரிப்பை உண்டாக்கும் கண்ணீர்புகைக் குண்டாகவும் பயன்படுகிறது.[2]
மேற்கோள்கள்
தொகு- ↑ "P-TOLUENESULFONYL CHLORIDE (TOSYL CHLORIDE)".
- ↑ 2.0 2.1 2.2 Whitaker, D. T. (2006). "p-Toluenesulfonyl Chloride". Encyclopedia of Reagents for Organic Synthesis. New York: John Wiley. DOI:10.1002/047084289X.rt136.pub2. பன்னாட்டுத் தரப்புத்தக எண் 978-0471936237.
- ↑ Ichikawa, J.; Nadano, R.; Mori, T.; Wada, Y. (2006). "5-endo-trig Cyclization of 1,1-Difluoro-1-alkenes: Synthesis of 3-Butyl-2-Fluoro-1-Tosylindole". Organic Syntheses 83: 111. http://www.orgsyn.org/demo.aspx?prep=v83p0111.; Collective Volume, vol. 11, p. 834
- ↑ Whitmore, F. C.; Hamilton, F. H. (1922). "Sodium Toluenesulfinate". Organic Syntheses 2: 89. http://www.orgsyn.org/demo.aspx?prep=CV1P0492.; Collective Volume, vol. 1, p. 492
- ↑ Lindner, O.; Rodefeld, L. (2005), "Benzenesulfonic Acids and Their Derivatives", Ullmann's Encyclopedia of Industrial Chemistry, Weinheim: Wiley-VCH, எண்ணிம ஆவணச் சுட்டி:10.1002/14356007.a03_507