பிரீட்லேன்டர் தொகுப்புவினை
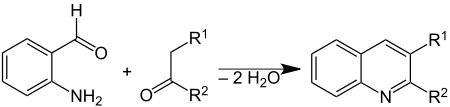
பிரீட்லேன்டர் தொகுப்புவினை (Friedländer synthesis) என்பது 2-அமினோபென்சால்டிகைடு சேர்மம் கீட்டோன்களுடன் வினைபுரிந்து குயினோலின் வழிபெறுதிகள் உருவாகும் வேதி வினையாகும்[1] with ketones to form quinoline derivatives.[2][3]. செருமானிய வேதியியலாளர் பால் பிரீட்லேன்டர் (1857–1923) இவ்வினையைக் கண்டறிந்ததால் அவரை சிறப்பிக்கும் வகையில் இவ்வினைக்கு பிரீட்லேன்டர் தொகுப்புவினை எனப்பெயரிடப்பட்டது.
| பிரீட்லேன்டர் தொகுப்புவினை | |
|---|---|
| பெயர் மூலம் | பால்பிரீலேன்டர் |
| வினையின் வகை | வளையம் உருவாகும் வினை |
| இனங்காட்டிகள் | |
| கரிமவேதியியல் வலைவாசல் | friedlaender-synthesis |
பிரீட்லேன்டர் தொகுப்புவினையானது முப்புளோரோஅசிட்டிக் அமிலம் [4], தொலுயீன்சல்போனிக் அமிலம்[5], அயோடின் [6] மற்றும் லூயிசு அமிலம் [7] ஆகிய வினையூக்கிகளின் துணையோடு நிகழ்கிறது. வினையைப் பற்றிய பல்வேறு விமர்சனங்கள் வெளியிடப்பட்டன[8][9][10].
வினைவழிமுறை
தொகுபிரீட்லேன்டர் தொகுப்புவினைக்கு இரண்டு வினைவழி முறைகள் சாத்தியமாகின்றன. முதலாவது வினைவழி முறையில் 2-அமினோபதிலீடு கார்பனைல் சேர்மம் 1 மற்றும் கார்பனைல் சேர்மம் 2 ஆகியவை வினைவீதத்தை உறுதிசெய்யும் படிநிலை வழியாக ஆல்டால் கூட்டு விளைபொருளாக 3 உருவாகின்றன. உருவான இந்த இடைநிலை விளைபொருள் நீக்கல் வினை மூலம் தண்ணீரை இழந்து நிறைவுறா கார்பனைல் சேர்மம் 4 உருவாகிறது. பின்னர் மீண்டும் ஒருமுறை இமைனிலிருந்து தண்ணீரை இழந்து குயினோலினாக 7 உருவாகிறது.
இரண்டாவது வினைவழி முறையில் முதலாவது படிநிலை சிகிப் காரம் விளைபொருள் 5 ஆக உருவாகி தொடர்ந்து ஆல்டால் வினையும் 6 மற்றும் நீக்கல் வினையும் நிகழ்ந்து 7 விளைபொருள் உருவாகிறது [11]
மேற்கோள்கள்
தொகு- ↑ Organic Syntheses, Coll. Vol. 3, p. 56 (1955); Vol. 28, p. 11 (1948). (Article)
- ↑ Friedländer, P. (1882). "Ueber o-Amidobenzaldehyd". Chemische Berichte 15 (2): 2572–2575. doi:10.1002/cber.188201502219.
- ↑ Friedländer, P.; Gohring, C. F. (1883). "Ueber eine Darstellungsmethode im Pyridinkern substituirter Chinolinderivate". Ber. 16 (2): 1833–1839. doi:10.1002/cber.18830160265.
- ↑ Shaabani, A.; Soleimani, E.; Badri, Z. (2007). "Triflouroacetic Acid as an Efficient Catalyst for the Synthesis of Quinoline". Synthetic Communications 37 (4): 629–635. doi:10.1080/00397910601055230.
- ↑ Jia, C.-S.; Zhang, Z.; Tu, S.-J.; Wang, G.-W. (2006). "Rapid and efficient synthesis of poly-substituted quinolines assisted by p-toluene sulphonic acid under solvent-free conditions: Comparative study of microwave irradiation versus conventional heating". Org. Biomol. Chem. 4: 104–110. doi:10.1039/b513721g.
- ↑ Wu, J.; Xia, H.-G.; Gao, K. (2006). "Molecular iodine: A highly efficient catalyst in the synthesis of quinolines via Friedländer annulation". Org. Biomol. Chem. 4: 126–129. doi:10.1039/b514635f.
- ↑ Varala, R.; Enugala, R.; Adapa, S. R. (2006). "Efficient and Rapid Friedlander Synthesis of Functionalized Quinolines Catalyzed by Neodymium(III) Nitrate Hexahydrate". Synthesis 2006: 3825–3830. doi:10.1055/s-2006-950296. https://archive.org/details/sim_synthesis_2006-11_22/page/3825.
- ↑ Manske, R. H. (1942). "The Chemistry of Quinolines". Chem. Rev. 30: 113–144. doi:10.1021/cr60095a006.
- ↑ Bergstrom, F. W. (1944). "Heterocyclic Nitrogen Compounds. Part IIA. Hexacyclic Compounds: Pyridine, Quinoline, and Isoquinoline". Chem. Rev. 35 (2): 77–277. doi:10.1021/cr60111a001.
- ↑ Cheng, C.-C.; Yan, S.-J. (2004). "The Friedländer Synthesis of Quinolines". Organic Reactions. எண்ணிம ஆவணச் சுட்டி:10.1002/0471264180.or028.02. பன்னாட்டுத் தரப்புத்தக எண் 0471264180.
- ↑ Jose Marco-Contelles; Elena Perez-Mayoral; Abdelouahid Samadi; Marıa do Carmo Carreiras; Elena Soriano (2009). "Recent Advances in the Friedlander Reaction". Chemical Reviews 109 (6): 2652–71. doi:10.1021/cr800482c. பப்மெட்:19361199.