சிர்கோனியம் டெட்ராபுளோரைடு
சிர்கோனியம் (IV) புளோரைடு, ZrF4 என்ற மூலக்கூறு வாய்பாட்டை உடைய ஒரு கனிம வேதிச் சேர்மம் ஆகும். இச்சேர்மம் ZBLAN எனப்படும் புளோரைடு கண்ணாடியின் ஒரு பகுதிப் பொருளாகும். இச்சேர்மம் தண்ணீரில் கரையாத தன்மை உடையது. இச்சேர்மம், புளோரோசிர்கோனேட் கண்ணாடிகளின் முக்கியமான பகுதிப்பொருளாகவும் உள்ளது.

| |
| பெயர்கள் | |
|---|---|
| ஐயூபிஏசி பெயர்s
சிர்கோனியம் (IV) புளோரைடு
சிர்கோனியம் டெட்ராபுளோரைடு | |
| இனங்காட்டிகள் | |
| 7783-64-4 15298-38-1 (ஒற்றைஐதரேட்) | |
| ChemSpider | 74196 |
| யேமல் -3D படிமங்கள் | Image |
| |
| பண்புகள் | |
| ZrF4 | |
| வாய்ப்பாட்டு எடை | 167.21 கி/மோல் |
| தோற்றம் | வெண்மை நிறப் படிகத்துாள் |
| அடர்த்தி | 4.43 கி/செமீ3 (20 °C) |
| உருகுநிலை | 910 °C (1,670 °F; 1,180 K) |
| 1.32 கி/100மிலி (20 °செ) 1.388 கி/100மிலி (25 °செ) | |
| கட்டமைப்பு | |
| படிக அமைப்பு | ஒற்றைச்சாய்வு, mS60 |
| புறவெளித் தொகுதி | C12/c1, No. 15 |
| தீங்குகள் | |
| தீப்பற்றும் வெப்பநிலை | தீப்பற்றாதது |
| Lethal dose or concentration (LD, LC): | |
LD50 (Median dose)
|
98 மிகி/கிகி (oral, mouse) 98 மிகி/கிகி (oral, rat)[1] |
| தொடர்புடைய சேர்மங்கள் | |
| ஏனைய எதிர் மின்னயனிகள் | சிர்கோனியம்(IV) குளோரைடு சிர்கோனியம்(IV) புரோமைடு சிர்கோனியம்(IV) அயோடைடு |
| ஏனைய நேர் மின்அயனிகள் | டைடானியம்(IV) புளோரைடு ஆப்னியம்(IV) புளோரைடு |
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |
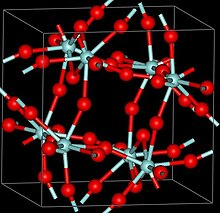
ZrF4 சேர்மத்திற்கு மூன்று படிக நிலைகள் அறியப் பட்டுள்ளன. அவை, α (ஒற்றைச் சாய்வு), β (நான்முகி, பியர்சன் குறியீடு tP40, தளவெளிக்குழு P42/m, எண். 84) மற்றும் γ (அறியப்படாத வடிவம்). β மற்றும் γ நிலைகள் நிலைத்தன்மையற்றவையாகவும், மேலும் 400 °செ வெப்பநிலையில், மீண்டும் மாற இயலாத மாற்றத்தின் மூலம் α வடிவம் அல்லது நிலைக்கு மாற்றமும் அடைகின்றன.[2]
வடித்திறக்கல் அல்லது பதங்கமாதல் முறையைப் பயன்படுத்தி சிர்கோனியம் புளோரைடை துாய்மைப்படுத்தலாம்.[3]
தவிர்க்கப்பட வேண்டிய நிலைகள் மற்றும் பொருட்கள்: ஈரப்பசை, செயலுறு உலோகங்கள், காடிகள் மற்றும் ஆக்சிசனேற்றிகள்.
பயன்கள்
தொகு- உலோக உற்பத்தி போன்ற ஆக்சிசனுக்கு எளிதில் துலங்கக்கூடிய வினைகளில் சிர்கோனியம் புளோரைடானது, சிர்கோனிய மூலமாகப் பயன்படுகிறது.[4]
- சிர்கோனியம் புளோரைடு மற்ற புளோரைடுகளுடன் கலந்தத கலவையில் உருகிய உப்பு உலைகளில் குளிர்விப்பானாகப் பயன்படுகிறது.
- சோடியம் புளோரைடுடனான கலவையில் இது உயர் வெப்பநிலை உலைகளுக்கான தனித்துவமிக்க குளிர்விப்பானாகப் பயன்படுகிறது.
- யுரேனியம் உப்புடனான கலவையில் சிர்கோனியம் புளோரைடானது, உருகிய உப்பு உலைகளில், எரிபொருள் குளிர்விப்பானின் ஒரு பகுதிப்பொருளாகப் பயன்படுகிறது.
- சோடியம் புளோரைடு, சிர்கோனியம் புளோரைடு மற்றும் யுரேனியம் டெட்ரா புளோரைடு கலந்த கலவை (53-41-6 மோல்.%) வானுார்தி உலை சோதனையில் குளிர்விப்பானாகப் பயன்படுகிறது.
- லித்தியம் புளோரைடு, பெரிலியம் புளோரைடு, சிர்கோனியம் புளோரைடு மற்றும் யுரேனியம்-233 டெட்ராபுளோரைடு ஆகியவற்றின் கலவை உருகிய உப்பு உலை சோதனையில் பயன்படுகிறது.(தோரியம் எரிபொருள் சுழற்சி உலைகளில் யுரேனியம்-233 பயன்படுகிறது)
மேற்கோள்கள்
தொகு- ↑ "Zirconium compounds (as Zr)". Immediately Dangerous to Life and Health. National Institute for Occupational Safety and Health (NIOSH).
- ↑ Paul L. Brown; Federico J. Mompean; Jane Perrone; Myriam Illemassène (2005). Chemical thermodynamics of zirconium. Gulf Professional Publishing. p. 144. பன்னாட்டுத் தரப்புத்தக எண் 0-444-51803-7.
- ↑ "Method for preparing ultra-pure zirconium and hafnium tetrafluorides. United States Patent 4578252". பார்க்கப்பட்ட நாள் 2009-07-07.
- ↑ "Zirconium fluoride". American Elements. பார்க்கப்பட்ட நாள் 2009-07-07.