மெத்தில் பைசல்பேட்டு
மெத்தில் பைசல்பேட்டு (Methyl bisulphate) என்பது CH4O4S என்ற மூலக்கூற்று வாய்ப்பாடு கொண்ட ஒரு வேதிச்சேர்மம் ஆகும். கந்தக அமிலத்தினுடைய ஒற்றை-மெத்தில் எசுத்தரான மெத்தில் பைசல்பேட்டு, இருமெத்தில் சல்பேட்டை ((CH3)2SO4 ) நீராற்பகுப்பு செய்யும் போது இடைநிலை விளைபொருளாக உருவாகிறது:[1].
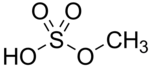
| |
| |
| பெயர்கள் | |
|---|---|
| வேறு பெயர்கள்
மெத்தில் சல்பேட்டு; மெத்தில்கந்தக அமிலம்; மெத்தில் ஐதரசன் சல்பேட்டு; ஒற்றை மெத்தில்சல்பேட்டு
| |
| இனங்காட்டிகள் | |
| 75-93-4 | |
| ChEBI | CHEBI:17760 |
| ChemSpider | 6172 |
| EC number | 201-058-1 |
InChI
| |
| யேமல் -3D படிமங்கள் | Image |
| KEGG | C00200 |
| பப்கெம் | 6412 |
| |
| பண்புகள் | |
| CH4O4S | |
| வாய்ப்பாட்டு எடை | 112.10 g·mol−1 |
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |
- (CH3)2SO4 + H2O → (CH3)HSO4 + CH3OH
மெத்தில் பைசல்பேட்டு ஒர் அமிலமாகும்.
- (CH3)HSO4 → (CH3)SO4− + H+
1993 ஆம் ஆண்டு மெத்தில் பைசல்பேட்டு கண்டறியப்பட்டு பரவலாக்கப்பட்டது. மீத்தேனை சில பாதரசச் சேர்மங்கள் முன்னிலையில், தெரிவுத்திறன் மிக்க அடர் கந்தக அமிலத்துடன் சேர்க்கும் போது மெத்தில் பைசல்பேட்டு உருவாகிறது. இங்கு பாதரசச் சேர்மங்கள் வினையூக்கியாகச் செயல்படுகின்றன[2]. எனினும், பாதரசச் சேர்மங்களின் நச்சுத்தன்மை காரணமாக 1998 ஆம் ஆண்டு வரையில் மெத்தில் பைசல்பேட்டு தயாரிப்பு தடைபட்டிருந்தது. பிளாட்டினம் அணைவுச்சேர்மங்கள் வினையூக்கியாக செயல்படுவது அறியப்பட்ட பின்னர், மீத்தேன் SO3 மற்றும் O2 வாயுக்களால் மெத்தில் பைசல்பேட்டாக மாற்றப்பட்டது. இதைத்தொடர்ந்து இச்சேர்மத்தின் பயன்பாடுகள் வெளிச்சத்திற்கு வந்தன[3][4][5]
- CH4 + SO3 + 1/2 O2 → (CH3)HSO4
இயற்கையில் பெருமளவு கிடைக்கும் மீத்தேன் வாயுவை, குறைந்த செலவில் அதிகப்பயனுடைய மெத்தனாலாக மாற்றுவதற்கான ஒரு தயாரிப்பு முறைக்கு மேற்கண்ட இந்தகண்டுபிடிப்பு வழிவகுத்தது. இச்செயல்முறையானது Pt-CH3 தொகுதி வழியாக மேற்கொள்ளப்பட வேண்டும் என்று முன்மொழியப்பட்டது[6].
(CH3)SO4− அயனியைக் கொண்டுள்ள உப்புகள் பொதுவாக வர்த்தகரீதியாகக் கிடைக்கின்றன, உதாரணம்: திரிசு(2-ஐதராக்சியெத்தில்)மெத்திலமோனியம் மெத்தில்சல்பேட்டு (CAS #29463-06-7).
மேற்கோள்கள்
தொகு- ↑ Robertson, R. E.; Sugamon, S.E. (1966). "The Hydrolysis of Dimethyl Sulfate and Diethyl Sulfate in Water". Canadian Journal of Chemistry 44 (14): 1728–1730. doi:10.1139/v66-260.
- ↑ Periana, R.A.; Taube, D.J.; Evitt, E.R.; Loffler, D.G.; Wentrcek, P.R.; Voss, G.; Masuda, T. (1993). "A Mercury-Catalyzed, High-Yield System for the Oxidation of Methane to Methanol". Science 259 (5093): 340–343. doi:10.1126/SCIENCE.259.5093.340. பப்மெட்:17832346.
- ↑ Hristov, I. H.; Ziegler, T. (2003). "The Possible Role of SO3 as an Oxidizing Agent in Methane Functionalization by the Catalytica Process. A Density Functional Theory Study". Organometallics 22 (8): 1668–1674. doi:10.1021/om020774j.
- ↑ Periana, R. A.; Mirinov, O.; Taube, D. J.; Gamble, S (2002). "High Yield Conversion of Methane to Methyl Bisulfate Catalyzed by Iodine Cations". Chemical Communications (20): 2376–2377. doi:10.1039/b205366g.
- ↑ Wolf, D. (1999). "High Yields of Methanol from Methane by C-H Bond Activation at Low Temperatures". Angewandte Chemie International Edition 37 (24): 3351–3353. doi:10.1002/(SICI)1521-3773(19981231)37:24<3351::AID-ANIE3351>3.0.CO;2-U.
- ↑ Periana, R. A.; Taube, D. J.; Gamble, S.; Taube, H.; Satoh, T.; Fujii, H. (1998). "Platinum Catalysts for the High-Yield Oxidation of Methane to a Methanol Derivative". Science 280 (5363): 560–564. doi:10.1126/science.280.5363.560. பப்மெட்:9554841.