கிளைசின்
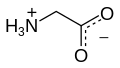
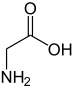
கிளைசின் (Glycine) [குறுக்கம்: Gly (அ) G][3] என்னும் அமினோ அமிலம் ஒரு கரிமச்சேர்மம் ஆகும். இதனுடைய வாய்பாடு: NH2CH2COOH. "பக்கத் தொடரில்" இரண்டு ஹைட்ரசன் அணுக்களை மட்டும் கொண்டுள்ளதால் புரதங்களில் சாதரணமாகக் காணப்படும் 20 அமினோ அமிலங்களில் கிளைசின் மிகவும் சிறியதாகவும், நீர்நாட்டமுள்ள மற்றும் நீர்தவிர்க்கும் இரண்டு சூழல்களிலும் பொருந்தக்கூடியதாகவும் உள்ளது. இதன் குறிமுறையன்கள்: GGU, GGC, GGA மற்றும் GGG. கிளைசின் வண்ணமற்ற, இனிய சுவையுள்ள படிகத்தன்மை கொண்ட திடப் பொருளாகும். இதற்கு சமச்சீரின்மை (chiral) பண்பு கிடையாது.
| |||
| |||
| பெயர்கள் | |||
|---|---|---|---|
| ஐயூபிஏசி பெயர்
கிளைசின்
| |||
| வேறு பெயர்கள்
அமினோ எதநோயிக் அமிலம்;
அமினோ அசெடிக் அமிலம் | |||
| இனங்காட்டிகள் | |||
| 56-40-6 | |||
| Abbreviations | Gly, G | ||
| ChEMBL | ChEMBL773 | ||
| ChemSpider | 730 | ||
| EC number | 200-272-2 | ||
IUPHAR/BPS
|
727 | ||
| யேமல் -3D படிமங்கள் | Image | ||
| KEGG | D00011 | ||
| பப்கெம் | 750 | ||
| |||
| UNII | TE7660XO1C | ||
| பண்புகள் | |||
| C2H5NO2 | |||
| வாய்ப்பாட்டு எடை | 75.07 | ||
| தோற்றம் | வெண்மையானத் திண்மம் | ||
| அடர்த்தி | 1.1607 கி/செ.மீ3 | ||
| உருகுநிலை | 233 °செ (சிதைதல்) | ||
| 24.99 கி/100 மிலி (25 °செ)[1] | |||
| கரைதிறன் | எதனோல், பிரிடீன்; ஈதரில் கரையாது | ||
| காடித்தன்மை எண் (pKa) | 2.34 (கார்பாக்சில்), 9.6 (அமினோ)[2] | ||
| தீங்குகள் | |||
| Lethal dose or concentration (LD, LC): | |||
LD50 (Median dose)
|
2600 mg/kg (mouse, oral) | ||
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |||
தயாரிப்பு மற்றும் முக்கியப் பண்புகள்
தொகுஹென்றி பிரகோன்னாட் என்னும் பிரெஞ்சு வேதியியலர் மற்றும் மருந்தாளுநர் 1820-ல் ஜெலாட்டினை கந்தக அமிலத்துடன் சேர்த்துக் கொதிக்கவைத்து கிளைசினைக் கண்டறிந்தார்[4].
தொழிலகங்களில் குளோரோ அசெடிக் அமிலத்துடன் அமோனியாவை வினைப்படுத்தி கிளைசின் தயாரிக்கப்படுகின்றது[5].
- ClCH2COOH + 2 NH3 → H2NCH2COOH + NH4Cl
இம்முறையில் சுமார் 15 மில்லியன் கிலோகிராம் கிளைசின் ஒரு வருடத்திற்கு உற்பத்திச் செய்யப்படுகிறது[6].
இதனுடையக் காடித்தன்மை எண்கள்: 2.35 மற்றும் 9.78. எனவே, அமிலக்காரக் குறியீடு (pH) 9.78 -ட்டிற்கு மேல் பெரும்பாலான கிளைசின் அமைன் எதிரயனிகளாக உள்ளது, H2NCH2CO2-. அமிலக்காரக் குறியீடு (pH) 2.35 -க்கு கீழே கிளைசின் கரைசல்கள் பெரும்பாலும் கார்பாக்சிலிக் அமில நேரயனிகளாகவே உள்ளது, H3N+CH2CO2H. இதனுடையச் சமமின்புள்ளி (pI): 6.06.
கிளைசின், கரைசல்களில் இருமுனை அயனி வடிவத்தில் உள்ளது. இவ்வடிவத்தில், பல அணுக்களிலும் உள்ள பகுதி மின்னூட்டங்களை காஸ்டெய்கர் மின்னூட்ட முறையில் கணக்கிடும்போது வரும் மதிப்புகள்: N (+0.2358), H (N- உடன் இணைந்தது) (+0.1964), ஆல்ஃபா-C (+0.001853), H (ஆல்ஃபா-C-யுடன் இணைந்தது) (+0.08799), கார்போனைல் C (+0.085) மற்றும் கார்போனைல் O (-0.5445).
உயிரித்தொகுப்பு
தொகுகிளைசின், நம் உணவில் தேவையில்லாதது. 3-பாஸ்போ கிளிசரேட்டிலிருந்து பெறப்பட்ட செரின் அமினோ அமிலத்திலிருந்து நம் உடல் உயிர்வேதியியல் முறையில் கிளைசினைத் தொகுத்துக் கொள்கிறது. பெரும்பாலான உயிரினங்களில் செரின் ஹைட்ராக்சி இடமாற்றி நொதி பிரிடாக்சால் பாஸ்பேட் என்னும் துணைக்காரணியின் உதவியுடன் வினையூக்கியாகச் செயல்பட்டு இவ்வுருமாற்றத்தை நிகழ்த்துகிறது:[7]
- செரின் + டெட்டிரா ஹைட்ரோஃபோலேட் → கிளைசின் + N5,N10-மெத்திலீன் டெட்டிரா ஹைட்ரோஃபோலேட் + H2O
முதுகெலும்புயிரிகளின் கல்லீரலில் கிளைசின் தொகுப்பி (மறு பெயர்: கிளைசின் பிளவு நொதி) என்னும் நொதியால் கிளைசின் தொகுக்கப்படுகின்றது. இத்தொகுப்பு மாற்றம் எளிதில் மீளுறும் தன்மையுள்ளது[7]
- CO2 + NH4+ + N5,N10-மெத்திலீன் டெட்டிரா ஹைட்ரோஃபோலேட் + NADH + H+ → கிளைசின் + டெட்டிரா ஹைட்ரோஃபோலேட் + NAD+
பெரும்பாலானப் புரதங்கள் கிளைசினைச் சிறிய அளவிலேயே கொண்டுள்ளன. ஆனால், 35% கிளைசினைக் கொண்ட கொலாஜென் புரதம் ஒரு குறிப்பிடத்தக்க விதிவிலக்காகும்[7].
சிதைவு
தொகுகிளைசின் மூன்று வழிகளில் சிதைக்கப்படுகிறது. விலங்குகளில், கிளைசின் சிதைவுத் தொகுதி நொதிகள் வினையூக்கத்தின் மூலம் கிளைசின் சிதைக்கப்படுவது முதன்மையான வழியாகும். இதே வினைவேகமாற்றிதான் கிளைசின் உயிரித்தொகுப்பிலும் ஈடுபடுகிறது. சிதைவு வழிமுறை, தொகுப்பு வழிமுறையின் தலைகீழ் வினையாகும்:[7]
- கிளைசின் + டெட்டிரா ஹைட்ரோஃபோலேட் + NAD+ → CO2 + NH4+ + N5,N10-மெத்திலீன் டெட்டிரா ஹைட்ரோஃபோலேட் + NADH + H+
இரண்டாவது வழிமுறையில் கிளைசின் இரு படிகளில் சிதைக்கப்படுகிறது. முதலாம் படியானது, செரின் அமினோ அமிலத்திலிருந்து செரின் ஹைட்ராக்சிமீத்தைல் இடமாற்றி நொதியின் உதவியுடன் நிகழும் உயிரிதொகுப்பின் தலைகீழ் வினையாகும். பின்னர் செரின், பைருவேட்டாக செரின் அமைன் நீக்கியால் மாற்றப்படுகிறது.[7]
மூன்றாவது வழிமுறையில் கிளைசின், அமினோ அமில உயிர்வளியேற்றி நொதியால் கிளையாக்சிலேட்டாக மாற்றப்படுகிறது. பின்னர், கிளையாக்சிலேட் ஈரலின் லேக்டேட் ஹைட்டிரசன் நீக்கியால் ஆக்சலேட்டாக NAD+-அய் சார்ந்த உயிர்வளியேற்றம் அடைகிறது.[7]
கிளைசினின் அரைச்சிதைவுக் காலமும், உடலிலிருந்து வெளியேற்றப்படுவதற்கான நேரமும் அதன் அளவைப் பொருத்தே முக்கியமாக அமைகிறது. ஒரு ஆய்வில், கிளைசினின் அரைச்சிதைவுக் காலம் 0.5 - 4.0 மணியாகக் கண்டறியப்பட்டது.[8]
மேற்கோள்கள்
தொகு- ↑ http://prowl.rockefeller.edu/aainfo/solub.htm
- ↑ Dawson, R.M.C., et al., Data for Biochemical Research, Oxford, Clarendon Press, 1959.
- ↑ IUPAC-IUBMB Joint Commission on Biochemical Nomenclature. "Nomenclature and Symbolism for Amino Acids and Peptides". Recommendations on Organic & Biochemical Nomenclature, Symbols & Terminology etc. பார்க்கப்பட்ட நாள் 2011-07-25.
- ↑ R.H.A. Plimmer (1912) [1908]. R.H.A. Plimmer & F.G. Hopkins (ed.). The chemical composition of the proteins. Monographs on biochemistry. Vol. Part I. Analysis (2nd ed.). London: Longmans, Green and Co. p. 82. பார்க்கப்பட்ட நாள் January 18, 2010.
- ↑ Ingersoll, A. W.; Babcock, S. H. (1932). "Hippuric acid". Organic Syntheses 12: 40. http://www.orgsyn.org/demo.aspx?prep=cv2p0328.; Collective Volume, vol. 2, p. 328.
- ↑ Karlheinz Drauz, Ian Grayson, Axel Kleemann, Hans-Peter Krimmer, Wolfgang Leuchtenberger, Christoph Weckbecker “Amino Acids” in Ullmann's Encyclopedia of Industrial Chemistry 2007, Wiley-VCH, Weinheim. எஆசு:10.1002/14356007.a02_057.pub2
- ↑ 7.0 7.1 7.2 7.3 7.4 7.5 A.L. Lehninger, D.L. Nelson and M.M.Cox (2008). Lehninger principles of biochemistry (5th ed.). New York: W.H. Freeman and Co. பார்க்கப்பட்ட நாள் July 25, 2011.[தொடர்பிழந்த இணைப்பு]
- ↑ Hahn RG (1993). "Dose-dependent half-life of glycine". Urological Research 21 (4): 289–291. doi:10.1007/BF00307714.