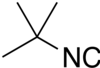
மூவிணைய பியூட்டைல் ஐசோசயனைடு
மூவிணைய பியூட்டைல் ஐசோசயனைடு (tert-Butyl isocyanide) என்பது Me3CNC (Me = மெதில், CH3) என்ற மூலக்கூற்று வாய்ப்பாட்டை உடைய ஒரு கரிமச் சேர்மம் ஆகும். C≡N-R என்ற வாய்ப்பாட்டால் குறிக்கப்படும் வினைசெயல் தொகுதியைக் கொண்டு கார்பைலமீன் அல்லது ஐசோநைட்ரைல் என அழைக்கப்படும் ஐசோ சயனைடாகும். மூவிணைய பியூட்டைல் ஐசோசயனைடு மற்ற அல்கைல் சயனைடுகளைப் போல், வினைத்திறன் மிக்க, நிறமற்ற, மிகவும் துர்நாற்றமுடைய ஒரு திரவமாகும். இது தாண்டல் உலோகங்களுடன் உலோக-கார்பன் வேதியியற் பிணைப்புகளில் ஈடுபட்டு நிலைத்தன்மையுடைய அணைவுச் சேர்மங்களை உருவாக்குகிறது.[1]
| |||
| பெயர்கள் | |||
|---|---|---|---|
| விருப்பத்தெரிவு ஐயூபிஏசி பெயர்
2-ஐசோசயனோ-2-மெதில்புரோப்பேன் | |||
| வேறு பெயர்கள்
t-BuNC
| |||
| இனங்காட்டிகள் | |||
| 7188-38-7 | |||
| ChemSpider | 22045 | ||
| யேமல் -3D படிமங்கள் | Image | ||
| பப்கெம் | 23577 | ||
| |||
| பண்புகள் | |||
| C5H9N | |||
| வாய்ப்பாட்டு எடை | 83.13 கி/மோல் | ||
| தோற்றம் | நிறமற்ற நீர்மம் | ||
| அடர்த்தி | 0.735 கி/செமீ3, திரவம் | ||
| கொதிநிலை | 91 °C (196 °F; 364 K) | ||
| பொருந்தாது | |||
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |||
மூவிணைய பியூட்டைல் ஐசோசயனைடானது ஆஃப்மன் கார்பைலமீன் வினையின் மூலம் தயாரிக்கப்படுகிறது. இந்த மாற்றத்தில், ஒரு டைக்குளோரோமீத்தேனில் கரைக்கப்பட்ட மூவிணைய பியூட்டைலமீனானது குளோரோஃபார்ம் மற்றும் நீரிய சோடியம் ஐதராக்சைடுடன் நிலைமாற்ற வினையூக்கியான பென்சைல்டிரைஎதில்அம்மோனியம் குளோரைடு முன்னிலையில் வினைபட்டு விளைபொருளானது கிடைக்கிறது.[2]
- Me3CNH2 + CHCl3 + 3 NaOH → Me3CNC + 3 NaCl + 3 H2O
மூவிணைய பியூட்டைல் ஐசோசயனைடானது மூவிணைய பியூட்டைல் சயனைடு என அழைக்கப்படும் பைவாலோநைட்ரைல் உடன் மாற்றியத்தைக் கொண்டுள்ளது. நைட்ரைல்கள் கார்பைலமீன் தொடரின் ஒத்த உறுப்புடன் கொண்டுள்ள வேறுபாடானது, CN வேதி வினைக்குழுவானது தாய் சேர்மத்துடன் இணைக்கப்பட்டுள்ள பிணைப்பானது கார்பன் மூலமானதாக அல்லாமல் நைட்ரசன் மூலமானதாக இருக்கும்.
அணைவுச் சேர்மங்களின் வேதியியல்
தொகுஅணைவுச் சேர்ம வேதியியலில், கார்பன் அணுவின் மீதான தனித்த எதிர்மின்னி இரட்டையின் பண்பின் காரணமாக, ஐசோசயனைடுகள், குறிப்பாக, 0, +1, மற்றும் +2 ஆக்சிசனேற்ற நிலைகளைக் கொண்ட உலோகங்களுடன் ஈந்தணைவிகளாக செயல்படுகின்றன. வழக்கமாக காணப்படும் ஆக்சிசனேற்ற நிலைகளைத் தவிரவும் கூட மூவிணைய பியூட்டைல் ஐசோசயனைடானது Pd(I) போன்றவற்றை நிலைத்தன்மை உடையதாக்க உதவுவதாக நிறுவப்பட்டுள்ளது.[3]
- Pd(dba)2 + PdCl2(C6H5CN)2 + 4 t-BuNC → [(t-BuNC)2PdCl]2 + 2 dba + 2 C6H5CN
மூவிணைய பியூட்டைல் ஐசோசயனைடானது மூவிணைய பியூட்டைல் போன்ற பெரிய தொகுதியைக் கொண்டதாகவும், M-C≡N-C பிணைப்புகளின் நேர்கோட்டுத்தன்மையின் காரணமாக, மைய உலோக அணுவிலிருந்து மிக அதிகமான துாரத்திலிருப்பினும் கூட, எப்டா-அணைவு ஒரே வகை ஈந்தணைவிகளைக் கொண்ட அணைவுச்சேர்மங்களை உருவாக்க முடியும்.[4]
உலோக கார்போனைல்களுடன் ஒத்த தன்மை
தொகுமூவணைய பியூட்டைல் ஐசோசயனைடானது விகிதாச்சார இயல்பின்படி ஈரணு உலோக கார்போனைல் அணைவுச்சேர்மங்களின் தொடரில் ஒத்த இடத்தில் உள்ளவற்றுடன் ஒத்த தன்மையைக் கொண்ட அணைவுச்சேர்மங்களை உருவாக்குகிறது. உதாரணமாக Fe2(CO)9 மற்றும் Fe2(tBuNC)9 ஆகியவற்றைக் குறிப்பிடலாம்.[5] அமைப்பு வாய்ப்பாட்டின்படி ஒத்தவையாக இருந்தாலும், ஒத்த கார்போனைல்கள் பல வழகளில் வேறுபடுகின்றன. முக்கியமாக t-BuNC ஆனது CO ஈந்தணைவியை விட சிறந்த ஈந்தணைவியாகும். ஆகையால், Fe(tBuNC)5 ஆனது எளிதாக புரோட்டானேற்றமடைகிறது. அதே நேரத்தில், அதனையொத்த கார்போனைல் சேர்மமான t Fe(CO)5 புரோட்டானேற்மடைவதில்லை.[6]
உலோக-கார்பன் வேதியியற் பிணைப்பில் உட்செருகுதல்
தொகுகுறிப்பிட்ட சில சூழல்களில், மூவிணைய பியூட்டை ஐசோசயனைடானது உலோக-கார்பன் பிணைப்புகளுக்குள் உட்செருகப்பட்டு இமினோஅசைல்களை உருவாக்குவதாகக் காட்டப்பட்டுள்ளது. ஐசோசயனைடுகளானவை உலோக-கார்பன் பிணைப்புகளினுாடாக உட்செருகப்படுதலானது கரிமத் தொகுப்பு முறைகளில் வலிமையான தொடர்பினைக் கொண்டுள்ளது.[7]
பாதுகாப்பு
தொகுமூவிணைய பியூட்டைல் ஐசோசயனைடானது நச்சுத்தன்மை வாய்ந்தது. கார்பனோராக்சைடுடன் நெருங்கிய எதிர்மின்னி அமைப்பு ரீதியாக ஒரே மாதிரியாக இருப்பதால் இச்சேர்மத்தின் இயல்பு கார்பனோராக்சைடுடன் ஒத்ததாக உள்ளது.
மேற்கோள்கள்
தொகு- ↑ Malatesta, L. Isocyanide Complexes of MetalsProgress in Inorganic Chemistry, 1959, volume 1, 284-291.
- ↑ Gokel, G.W.; Widera, R.P.; Weber, W.P. (1988). "Phase-transfer Hofmann carbylamine reaction: tert-butyl isocyanide". Organic Syntheses. http://www.orgsyn.org/demo.aspx?prep=CV6P0232.; Collective Volume, vol. 6, p. 232CS1 maint: Multiple names: authors list (link)Gokel, G.W.; Widera, R.P.; Weber, W.P. (1988). "Phase-transfer Hofmann carbylamine reaction: tert-butyl isocyanide". Organic Syntheses. http://www.orgsyn.org/demo.aspx?prep=CV6P0232.; Collective Volume, vol. 6, p. 232
- ↑ Rettig, M.F.; Maitlis, P.M.; Cotton, F.A.; Webb, T.R. Tetrakis(tert-butyl isocyanide)Di-μ-chloro-dipalladium(I). Inorganic Syntheses, 1990, 28, 110-113. பன்னாட்டுத் தரப்புத்தக எண் 0-470-13259-00-470-13259-0. எஆசு:10.1002/9780470132593.ch29
- ↑ Carnahan, E.M.; Protasiewicz, J.D.; Lippard, S.J. 15 years of reductive coupling: what have we learned? Acc. Chem. Res. 1993, 26, 90-97
- ↑ Bassett, J.M.; Barker, G.K.; Green, M.; Howard, J.A.; Stone, G.A.; Wolsey, W.C. "Chemistry of low-valent metal isocyanide complexes" J.C.S. Dalton, 1981, 219-227.
- ↑ Bassett, J.M.; Farrugia, L.J.; Stone, G.A. "Protonation of pentakis(t-butyl isocyanide)iron" J.C.S. Dalton, 1980, 1789-1790.
- ↑ Vicente, J; Abad, J.A.; Fortsch, W.; Lopez-Saez, M.J. Reactivity of ortho-palladated phenol derivatives with unsaturated molecules. Organometallics, 2004, 23, 4414-4429. DOI 10.1021/om0496131.