இருகந்தகம்
இருகந்தகம் (Disulfur) என்பது S2.[1] என்ற மூலக்கூற்று வாய்ப்பாட்டால் விவரிக்கப்படும் ஓர் ஈரணு மூலக்கூறாகும். ஈராக்குசிசன் மூலக்கூறுக்கு ஒத்ததாக இருகந்தகமும் இருக்கிறது ஆனால் அறை வெப்பநிலையில் இருகந்தகம் அரிதாகவே தோன்றுகிறது. ஊதா நிறத்திலுள்ள இந்த வளிமம் சூடான கந்தக நீராவிகளில் ஆதிக்கம் செலுத்துகிறது. ஐஓ சந்திரனின் வளிமண்டலத்தில் காணப்படும் சிறிய உட்கூறுகளில் இருகந்தகமும் ஒன்றாகும். வியாழன் கோளுக்குரிய சந்திரனான ஐஓவில் முக்கியமாக SO2 உள்ளடங்கியுள்ளது. [2] இருகந்தகத்தின் உறுதியற்ற நிலைப்புத்தன்மை பொதுவாக இரட்டைப் பிணைப்பு விதியின் பின்னணியில் விவரிக்கப்படுகிறது.
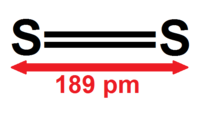
| |
| |
| பெயர்கள் | |
|---|---|
| ஐயூபிஏசி பெயர்
இருகந்தகம்
| |
| வேறு பெயர்கள்
ஈரணு கந்தகம்
கந்தகம் | |
| இனங்காட்டிகள் | |
| 23550-45-0 | |
| ChEBI | CHEBI:29387 |
| ChemSpider | 4574100 |
Gmelin Reference
|
753 |
| யேமல் -3D படிமங்கள் | Image |
| பப்கெம் | 5460602 |
| |
| பண்புகள் | |
| S2 | |
| வாய்ப்பாட்டு எடை | 64.12 g·mol−1 |
| இருமுனைத் திருப்புமை (Dipole moment) | 0 D |
| வெப்பவேதியியல் | |
| Std enthalpy of formation ΔfH |
128.60 கிலோயூல் மோல்−1 |
| நியம மோலார் எந்திரோப்பி S |
228.17 யூல் கெல்வின்−1மோல்−1 |
| வெப்பக் கொண்மை, C | 32.51 கிலோயூல் கெல்வின்−1 மோல்−1 |
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |
தயாரிப்பு
தொகு530° செல்சியசு வெப்பநிலையும் 1மில்லிமீட்டர் குறைந்த அழுத்தமும் கொண்ட கந்தகத்தை 720° செல்சியசு வெப்பநிலைக்கு சூடுபடுத்தினால் ஊதாநிறமுள்ள இருகந்தக வளிமம் உருவாகிறது. கார்பனைல் சல்பைடின் வளிமண்டலத்தை பாதரச ஒளியுணர்வு மிகைப்பியைப் பயன்படுத்தி புற ஊதா ஒளியுடன் கதிர்வீச்சுக்கு உட்படுத்தும்போதும் அல்லது CS2, H2S2, S2Cl2 அல்லது C2H4S, PSF3 அல்லது COS போன்றவற்றை கதிர்வீச்சுக்கு உட்படுத்தும்போதும் இருகந்தகம் தயாரிக்கப்படுகிறது. [3]
இயற்கையில் இருகந்தகம்
தொகுவியாழனின் சந்திரன் ஐஓவின் மேற்பரப்பில் பீலே எரிமலைக்கு அருகில் இருந்து உமிழப்படும் வளிமத்தில் இருகந்தகம் கண்டறியப்பட்டுள்ளது. [4]
பண்புகள்
தொகுS2 இன் அடிநிலை ஒரு மும்மையாகும். O2 மற்றும் SO போன்ற இணைக்கப்படாத இரண்டு எலக்ட்ரான்கள் இந்த ஈரியங்குருபில் உள்ளன. S-S 189 பைக்கோமீட்டர் பிணைப்பு இடைவெளியை S-S பிணைப்பு பெற்றுள்ளது. S8 இல் இடம்பெற்றுள்ள 206 பைக்கோமீட்டர் பிணைப்பு இடைவெளி கொண்ட S-S ஒற்றைப் பிணைப்புகளை விட இது நீளம் குறைந்ததாகும். இருகந்தகம் 715 செ.மீ−1 இல் இராமன் நிறமாலை அதிர்வெண்பட்டையில் அடையாளம் காணப்படுகிறது. [5] தொடர்புடைய ஆக்குசிசனின் O-O மூலக்கூறு 1556 செ.மீ−1 இல் அடையாளம் காணப்படுகிறது. [6] S-S மூலக்கூறின் பிணைப்பு ஆற்றல் 430 கிலோயூல்/மோல் ஆகும். இதேபோல தொடர்புடைய ஆக்சிசன் மூலக்கூறின் பிணைப்பு ஆற்றல் 498 கிலோயூல்/மோல் ஆகும். [7] சூரிய ஒளியில் 7.5 நிமிடம் சராசரி ஆயுட்காலம்[8] கொண்ட இருகந்தகம் உடனடியாக ஒளியணுக்களால் ஒளிப்பிரிகை அடைகிறது. [9]
மேற்கோள்கள்
தொகு- ↑ Steudel, Ralf; Eckert, Bodo (2003). "Solid Sulfur Allotropes". Elemental Sulfur and Sulfur-Rich Compounds I. Topics in Current Chemistry. Vol. 230. pp. 58–68. எண்ணிம ஆவணச் சுட்டி:10.1007/b12110. பன்னாட்டுத் தரப்புத்தக எண் 978-3-540-40191-9.
- ↑ Lellouch, E. (January 2005). "Io's Atmosphere and Surface-Atmosphere Interactions". Space Science Reviews 116 (1–2): 211–224. doi:10.1007/s11214-005-1957-z. Bibcode: 2005SSRv..116..211L.
- ↑ Tardif, Sylvie L.; Rys, Andrzej Z.; Abrams, Charles B.; Abu-Yousef, Imad A.; Lesté-Lasserre, Pierre B. F.; Schultz, Erwin K. V.; Harpp, David N. (1997). "Recent chemistry of the chalcogen diatomics". Tetrahedron 53 (36): 12225–12236. doi:10.1016/S0040-4020(97)00555-3. https://archive.org/details/sim_tetrahedron_1997-09-08_53_36/page/n180.
- ↑ Spencer, J. R. (2000). "Discovery of Gaseous S2 in Io's Pele Plume". Science 288 (5469): 1208–1210. doi:10.1126/science.288.5469.1208. பன்னாட்டுத் தர தொடர் எண்:0036-8075. பப்மெட்:10817990. Bibcode: 2000Sci...288.1208S.
- ↑ Eckert, Bodo; Steudel, Ralf (2003). "Molecular Spectra of Sulfur Molecules and Solid Sulfur Allotropes". Elemental Sulfur and Sulfur-Rich Compounds II. Topics in Current Chemistry. Vol. 231. pp. 181–191. எண்ணிம ஆவணச் சுட்டி:10.1007/b13181. பன்னாட்டுத் தரப்புத்தக எண் 978-3-540-40378-4.
- ↑ Hill, R.A.; Esherick, P.; Owyoung, A. (1983). "High-resolution stimulated Raman spectroscopy of O2" (in en). Journal of Molecular Spectroscopy 100 (1): 119–133. doi:10.1016/0022-2852(83)90029-2.
- ↑ (Lide, David R., ed. (2006). CRC Handbook of Chemistry and Physics (87th ed.). Boca Raton, FL: CRC Press. பன்னாட்டுத் தரப்புத்தக எண் 0-8493-0487-3.
- ↑ Ahearn, M. F.; Schleicher, D. G.; Feldman, P. D. (1983). "The discovery of S2 in comet IRAS-Araki-Alcock 1983d". The Astrophysical Journal 274: L99. doi:10.1086/184158. பன்னாட்டுத் தர தொடர் எண்:0004-637X. Bibcode: 1983ApJ...274L..99A.
- ↑ Frederix, Pim W. J. M.; Yang, Chung-Hsin; Groenenboom, Gerrit C.; Parker, David H.; Alnama, Koutayba; Western, Colin M.; Orr-Ewing, Andrew J. (2009). "Photodissociation Imaging of Diatomic Sulfur (S2)†". The Journal of Physical Chemistry A 113 (52): 14995–15005. doi:10.1021/jp905104u. பன்னாட்டுத் தர தொடர் எண்:1089-5639. பப்மெட்:19754091. Bibcode: 2009JPCA..11314995F.
புற இணைப்பு
தொகு- பொதுவகத்தில் இருகந்தகம் தொடர்பாக ஊடகக் கோப்புகள் உள்ளன.