சர்க்கரைச் சிதைவு
இக்கட்டுரை கூகுள் மொழிபெயர்ப்புக் கருவி மூலம் உருவாக்கப்பட்டது. இதனை உரை திருத்த உதவுங்கள். இக்கருவி மூலம்
கட்டுரை உருவாக்கும் திட்டம் தற்போது நிறுத்தப்பட்டுவிட்டது. இதனைப் பயன்படுத்தி இனி உருவாக்கப்படும் புதுக்கட்டுரைகளும் உள்ளடக்கங்களும் உடனடியாக நீக்கப்படும் |
சர்க்கரைச் சிதைவு (குளுக்கோஸுக்கான பழைய சொல்லான[1] கிளைக்கோஸ் , + -லைசிஸ் சிதைவு; கிளைகோலைஸிஸ்) என்பது வளர்சிதை மாற்ற வழிமுறை ஆகும், இது குளுக்கோஸ், C6H12O6 ஐ, பைருவேட், CH3COCOO− + H+ ஆக மாற்றுகிறது. இந்த செயல்முறையில் வெளிவிடப்படும் கட்டில்லாச் சக்தி உயர் சக்தி சேர்மங்களான, ATP (அடினோசின் டிரைபாஸ்பேட்) மற்றும் NADH (குறைக்கப்பட்ட நிக்கோட்டினமைடு அடினைன் டைநியூக்ளியோடைடு) ஆகியவற்றை உருவாக்கப் பயன்படுத்தப்படும்.
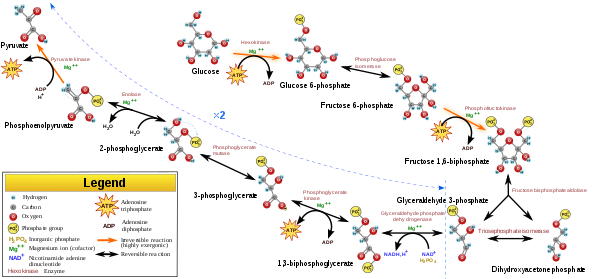
சர்க்கரைச் சிதைவு பத்து இடைநிலை சேர்மங்கள் பங்குகொள்ளும் ஒரு நிச்சயமான வரிசைமுறையிலமைந்த பத்து எதிர்வினைகளாகும் (படிகளில் ஒன்று இரு இடைநிலைகளில் ஈடுபடுகிறது). இடைநிலைகள் சர்க்கரைச் சிதைவிற்கான நுழைவுப் புள்ளியை வழங்குகின்றன. எடுத்துக்காட்டாக, ஃபுருக்டோஸ், குளுக்கோஸ் மற்றும் கேலக்டோஸ் போன்ற பெரும்பாலான ஒருசக்கரைட்டுகள் இந்த இடைநிலைகளில் ஒன்றாக மாற்றப்படலாம். இடைநிலைகள் நேரடியாகவும் பயனுள்ளதாக இருக்கக்கூடும். எடுத்துக்காட்டாக, டைஹைட்ராக்சிஅசட்டோன் பாஸ்பேட் இடைநிலையானது கொழுப்பை உருவாக்குவதற்காக கொழுப்பமிலங்களுடன் இணைகின்ற கிளிசரோலின் ஒரு மூலமாகும். (பத்மநாபன்)
சர்க்கரைச் சிதைவு உலகளாவிய வளர்சிதை மாற்ற வழிமுறையின் ஆதிவகையென எண்ணப்படுகிறது. இது கிட்டத்தட்ட காற்றுவாழ் மற்றும் காற்றின்றிவாழ் உயிரினங்கள் அனைத்திலும் வேறுபாடுகளுடன் நிகழ்கிறது. சர்க்கரைச் சிதைவு பரந்தளவில் நிகழுகையானது, பழையகாலத்தின் கூடியளவில் அறியப்பட்ட வளர்சிதை மாற்ற வழிமுறைகளில் ஒன்று என்பதைக் குறிக்கிறது.[2]
மிகவும் பொதுவான சர்க்கரைச் சிதைவு வகை Embden-Meyerhof-Parnus pathway ஆகும், இது முதன்முதலில் குஸ்டாவ் எம்ப்டென் மற்றும் ஒட்டோ மெயர்ஹொஃப் மற்றும் பார்னஸ் ஆகியோரால் கண்டுபிடிக்கப்பட்டது. சர்க்கரைச் சிதைவு Entner–Doudoroff pathway போன்ற பிற வழிமுறைகளையும் குறிப்பிடுகிறது. இருந்தபோதும் இங்குள்ள விவாதமானது எம்ப்டென்-மெயர்ஹொஃப் வழிமுறைக்குள் மட்டுப்படுத்தப்படும்.
சுருக்கம்
தொகுசர்க்கரைச் சிதைவின் ஒட்டுமொத்த எதிர்வினையாவது:
| D-[குளுக்கோஸ்] | [பைருவேட்] | ||||
| + 2 [NAD]+ + 2 [ADP] + 2 [P]i | 2 | + 2 [NADH] + 2 H+ + 2 [ATP] + 2 H2O |
இந்தச் சமன்பாட்டில் குறியீடுகளின் பயன்பாடானது உயிர்வளி அணுக்கள், ஹைட்ரஜன் அணுக்கள் மற்றும் ஏற்றங்கள் குறித்து சமநிலையற்ற தோற்றத்தை உண்டாக்கும். அணுச் சமநிலையானது இரு பாஸ்பேட் (Pi) குழுக்களால்[3] பேணப்படுகிறது:
- ஒவ்வொன்றும் ஹைட்ரசன் பாஸ்பேட் எதிரயன் (HPO42-) வடிவத்தில் இருக்கும், ஒட்டுமொத்தமாக 2 H+ ஐ வழங்க பிரிகின்றது
- ADP (அடினோசின் டைபாஸ்பேட்) மூலக்கூறுடன் இணையும்போது, ஒவ்வொன்றும் ஒரு உயிர்வளி அணுவை விடுவிக்கும், ஒட்டுமொத்தமக 2 O ஐ வழங்குகின்றது
ADP க்கும் ATP க்கும் இடையிலான வேறுபாட்டால் ஏற்றங்கள் சமப்படுத்தப்படுகின்றன. கலமுறைச் சூழலில் ADP இன் அனைத்து மூன்று ஹைட்ராக்சி குழுக்களும் -O- மற்றும் H+ ஆக பிரிகையடைந்து, ADP3- ஐ வழங்குகின்றன, மேலும் இந்த அயன் Mg2+ உடன் அயனுக்குரிய பிணைப்பில் இருக்கும், ADPMg- ஐ வழங்குகிறது. ATP இல் ATPMg2- ஐ வழங்குகின்ற நான்கு ஹைட்ராக்சி குழுக்கள் காணப்படுவது தவிர மற்றும்படி ஒரேமாதிரியே செயல்படுகிறது. இரண்டு பாஸ்பேட் குழுக்களிலுள்ள உண்மையான ஏற்றங்களுடன் இந்த வேறுபாடுகள் ஒன்றாகக் கருதப்படும்போது, ஒவ்வொரு பக்கத்திலுமுள்ள தேறிய ஏற்றங்கள் -4 சமப்படுத்தப்படுகின்றன.
எளிமையான காற்றின்றிவாழ் நொதித்தல்களில், ஒரு மூலக்கூறு குளுக்கோஸ் இரு பைருவேட் மூலக்கூறுகளாக வளர்சிதை மாற்றம் அடைதலில் இரு ATP மூலக்கூறுகள் தேறிய விளைவாகக் கிடைக்கின்றன. பயன்படுத்திய NAD+ ஐ 'மீளளிப்பதற்காக' அநேகமான கலங்கள் மேலும் எதிர்வினைகளை நடத்தி, இறுதித் தயாரிப்பாக எதனோல் அல்லது லக்டிக் அமிலத்தை உண்டாக்கும். பல பாக்டீரியாக்கள், NAD+ ஐ மறுஉற்பத்தி செய்வதற்கு அசேதன சேர்மங்களை ஹைட்ரஜன் ஏற்பிகளாகப் பயன்படுத்துகின்றன.
காற்றுவாழ் சுவாசத்தை மேற்கொள்கின்ற கலங்கள் அதிகளவான ATP ஐத் தொகுக்கின்றன, ஆனால் சர்க்கரைச் சிதைவின் ஒரு பகுதியாக அல்ல. இந்த மேலதிக காற்றுவாழ் எதிர்வினைகள் கிளைகோலைஸிலிருந்து வரும் பைருவேட் மற்றும் NADH + H+ ஐப் பயன்படுத்துகின்றன. யூக்கரியோடிக் காற்றுவாழ் சுவாசமானது, ஒவ்வொரு குளுக்கோஸ் மூலக்கூற்றுக்கும் கிட்டத்தட்ட 34 மேலதிக ATP மூலக்கூறுகளை உருவாக்கும், எனினும் இவற்றில் பலவும் கிளைகோலைஸிஸில் உள்ள தளப்பொருள்-நிலை பாஸ்ஃபோ ஏற்றத்தை விட பரந்தளவில் வேறுபட்ட பொறிமுறையால் உருவாக்கப்படுகின்றன.
கொழுப்பமிலங்கள் போன்ற காற்றின்றிவாழ்கின்ற-ஆக்ஸிஜன் ஏற்றக்கூடிய தளப்பொருள்களின் மாற்று மூலங்கள் காணப்பட்டால் அன்றி, காற்றுவாழ் சுவாசத்துடன் ஒப்பிடும்போது காற்றின்றிவாழ் சுவாசத்தின் குளுக்கோஸ் ஒன்றுக்கு குறைந்தளவு சக்தி உருவாக்கமானது ஹைபாக்ஸிக் (தாழ்-ஆக்சிஜன்) நிலமைகளின் கீழ் அந்த வழிமுறையினூடாக கூடுதலான பாயத்தை விளைவிக்கும்.
வழிமுறையின் விளக்கம்
தொகு1860 இல், நுண்ணுயிர்களே நொதித்தலுக்குப் பொறுப்பானவை என்பதை லூயிஸ் பாஸ்சர் கண்டுபிடித்தார். 1897 இல், சில கலங்களின் பிரித்தெடுப்புகள் நொதித்தலை உண்டுபண்ணலாம் என்பதை எடுவர்டு பூக்னர் கண்டுபிடித்தார். 1905 இல், ஆர்தர் ஹென்டர்சன் மற்றும் வில்லியம் யங் ஆகியோர், நொதித்தல் தொடர்ந்து நடப்பதற்கு வெப்பம்-உணரும் உயர்-மூலக்கூற்று-எடை உபகலமுறை பகுதி (நொதியங்கள்) மற்றும் வெப்பம்-உணரும் தாழ்-மூலக்கூற்று-எடை குழியமுதலுரு பகுதி (ADP, ATP மற்றும் NAD+ மற்றும் பிற துணைக்காரணிகள்) அனைத்தும் ஒன்றாகத் தேவைப்படுகின்றன என்று தீர்மானித்தனர். இந்த வழிமுறையின் விவரமானது கடைசியாக 1940 அளவில், ஒட்டோ மெயர்ஹொஃப் இலிருந்தான பிரதான உள்ளீட்டுடன் மற்றும் சில ஆண்டுகள் கழித்து லூயிஸ் லெலொய்ரால் தீர்மானிக்கப்பட்டது. வழிமுறையின் சிக்கல்களைத் தீர்மானிப்பதிலுள்ள மிகப்பெரிய சிரமங்கள் மிகக் குறுகிற வாழ்நாள் மற்றும் விரைவான சர்க்கரைச் சிதைவு எதிர்வினைகளின் இடைநிலைகளின் நிலையான-நிலை குறைந்த செறிவுகள் காரணமாக ஏற்பட்டது
எதிர்வினைகளின் வரிசை
தொகுஆயத்தக் கட்டம்
தொகுகுளுக்கோஸை மூன்று-கார்பன் சர்க்கரை பாஸ்பேட்டுகளாக (G3P) மாற்றுவதற்கு சக்தியை உள்ளெடுப்பதால், முதல் ஐந்து படிநிலைகளும் ஆயத்த (அல்லது முதலீட்டு) கட்டம் எனக் குறிப்பிடப்படும்.
| சர்க்கரைச் சிதைவின் முதல் படிநிலை, குளுக்கோஸ் 6-பாஸ்பேட் (G6P) ஐ உருவாக்க, ஹெக்ஸாகைனேஸ்கள் எனப்படுகின்ற ஒரு நொதியத் தொகுதியால் குளுக்கோஸின் பாஸ்ஃபோ ஏற்றம் நடைபெறுகிறது. இந்த வினையானது ATP ஐ உள்ளெடுக்கும், ஆனால் இது குளுக்கோஸ் செறிவைக் குறைவாக வைக்கவும், பிளாஸ்மா மென்படல கடத்திகளின் ஊடாக கலத்துக்குள் குளுக்கோஸ் தொடர்ச்சியாகக் கடத்தப்படுவதை மேம்படுத்தவும் செயல்படுகிறது. மேலதிகமாக, குளுக்கோஸ் வெளிக்கசிவதையும் தடுக்கும் - G6P க்கான கடத்திகள் கலத்தில் இல்லை. குளுக்கோஸானது மாற்றுவழியாக அககலமுறை மாச்சத்து அல்லது கிளைக்கோஜனின் பாஸ்பரோபகுப்பு அல்லது நீர்ப்பகுப்பிலிருந்து பெறப்படலாம்.விலங்குகளில், குளுக்கோகைனேஸ் எனப்படுகின்ற ஹெக்ஸோகைனேசின் ஐசோஸைம் ஈரலில் பயன்படுத்தப்படுகிறது, ஈரல் குளுக்கோஸுக்கு குறைந்தளவு நாட்டமுள்ளது (சாதாரண கிளைசீமியாவின் சமீபத்தில் Km), மற்றும் ஒழுக்காற்று பண்புகளில் வேறுபடுகிறது. குருதி சர்க்கரை மட்டங்களைப் பேணுவதில் ஈரலுக்குள்ள பங்கை இந்த நொதியத்தின் வேறுபட்ட தளப்பொருள் நாட்டமும், மாற்று ஒழுங்கமைப்பும் பிரதிபலிக்கின்றன.துணைக்காரணிகள்: Mg2+ |
| ||||||||||||||||||||
| G6P ஆனது பின்னர் குளுக்கோஸ் பாஸ்பேட் ஐசோமரேஸால் ஃபுருக்டோஸ் 6-பாஸ்பேட்டில் (F6P) மறு ஒழுங்குபடுத்தப்படும். இந்த இடத்தில் பாஸ்ஃபோ ஏற்றம் மூலமாக ஃபுருக்டோஸும் சர்க்கரைச் சிதைவு வழிமுறையில் நுழையலாம்.அமைப்பிலுள்ள மாற்றம் ஒரு சமபகுதியாகுதன்மை ஆகும், இதில் G6P ஆனது F6P ஆக மாற்றப்பட்டுள்ளது. எதிர்வினை தொடர்வதற்கு நொதியம், பாஸ்போஹெக்ஸோஸ் ஐசோமரேஸ் தேவை. இந்த எதிர்வினை சாதாரண கல நிலமைகளின் கீழ் கட்டின்றி மீளக்கூடியது. இருந்தபோதும், சர்க்கரைச் சிதைவின் அடுத்த படிநிலையின்போது தொடர்ச்சியாக உள்ளெடுக்கப்படுகின்ற F6P இன் செறிவு குறைவதன் காரணமாக பெரும்பாலும் முன்னோக்கி செலுத்தப்படுகிறது. உயர் F6P செறிவு நிலமைகளில், இந்த எதிர்வினை உடனும் பின்னோக்கி இயங்கும். இந்த தோற்றப்பாட்டை லி சாடிலியரின் கோட்பாடு மூலமாக விளக்கலாம். |
| ||||||||||||||||||||
| இந்த படிநிலையின் இன்னொரு ATP இன் சக்தி செலவளிப்பை 2 வழிகளில் சமர்த்திக்கலாம்: சர்க்கரைச் சிதைவின் செயல்முறை (இந்த படிநிலை வரை) மீளுந்தன்மையற்றது, வழங்கப்பட்ட சக்தி மூலக்கூற்றை நிலையற்றதாக்கும். ஏனெனில் பாஸ்போஃபுருக்டோகைனேஸ் 1 (PFK-1) தூண்டிய எதிர்வினையானது சக்திரீதியாக மிகச் சாதகமானது, இது மிகமுக்கியமாக மீளுந்தன்மையற்றது மற்றும் குளுக்கோசுப்புத்தாக்கம் நடக்கும்போது பின்னோக்கிய மாற்றத்தைச் செய்ய வேறுபட்ட வழிமுறை ஒன்றைப் பயன்படுத்தவேண்டும். இது வினையை ஒரு முக்கிய ஒழுங்காற்று நிலையாக மாற்றும் (கீழே பார்க்கவும்). இது ஒரு வீத கட்டுப்பாட்டு படிநிலையும் கூட. அதே வினையையும் பைரோபாஸ்பேட்டைச் சார்ந்த பாஸ்போஃபுருக்டோகைனேஸ் (PFP அல்லது PPi-PFK ) தூண்டக்கூடியது, இது பெரும்பாலான தாவரங்கள், சில பாக்டீரியாக்கள், ஆர்கியா மற்றும் புரோடிஸ்டுகள் ஆகியவற்றில் உள்ளது, ஆனால் விலங்குகளில் இல்லை. இந்த நொதியமானது பாஸ்பேட் வழங்கியாக ATP க்குப் பதில் பைரோபாஸ்பேட்டை (PPi) பயன்படுத்தும். இந்த மீளுந்தன்மையுள்ள வினையானது சர்க்கரைச் சிதைவு வளர்சிதை மாற்றத்தின் நெகிழ்தன்மையை அதிகரிக்கிறது.[4] அரிதான ADP - யைச் சார்ந்த PFK நொதிய மாறி ஆர்க்கியன் இனங்களில் அடையாளம் காணப்பட்டுள்ளது.[5]துணைக்காரணிகள்: Mg2+ |
| ||||||||||||||||||||
| முந்தைய எதிர்வினையிலுள்ள மூலக்கூற்றை நிலையற்றதாக்குவதானது, ஹெக்ஸோஸ் வளையத்தை ஆல்டொலேஸ் நொதியமானது இரண்டு டிரையோஸ் சர்க்கரைகளாக (கீட்டோனாக: டைஹைட்ராக்சிஅசட்டோன் பாஸ்பேட் மற்றும் அல்டிகைட்டாக: கிளிசரல்டிகைட் 3-பாஸ்பேட்) பிரிக்கும். இரண்டு வகுப்புகளில் அடங்கும் ஆல்டொலேஸ்கள் உள்ளன: பிரிவு (I) ஆல்டொலேஸ்கள் விலங்குகளிலும் தாவரங்களிலும் உள்ளன, பிரிவு (II) ஆல்டொலேஸ்கள் பூஞ்சைக்காளான் மற்றும் பாக்டீரியாவில் உள்ளன; இந்த இரண்டு வகுப்புகளிம் கீட்டோஸ் வளையத்தை பிளவுபடுத்துவதில் வேறுபட்ட பொறிமுறைகளைப் பயன்படுத்துகின்றன. |
| ||||||||||||||||||||||||||
| டிரையோஸ்பாஸ்பேட் ஐசோமரேஸ் ஆனது டைஹைட்ராக்சிஅசட்டோன் பாஸ்பேட்டை கிளிசரால்டிகைட் 3-பாஸ்பேட்டுடன் (GADP ) மிகத்துரிதமாக ஒன்றுக்கொன்று இடைமாற்றம் செய்யும், இது மேலும் சர்க்கரைச் சிதைவில் தொடரும். கிளிசரால்டிகைட் 3-பாஸ்பேட் போலவே டைஹைட்ராக்சிஅசட்டோன் பாஸ்பேட்டும் இதே வழிமுறையில் செல்ல வழிவகுப்பதால் நன்மையானதாகும். இது சீராக்கத்தை எளிமைப்படுத்துகிறது. |
| ||||||||||||||||||||
பயன்பெறு கட்டம்
தொகுசர்க்கரைச் சிதைவின் இரண்டாம் பாதி பயன்பெறு கட்டம் எனப்படுகிறது, இது சக்தி-சேமிப்பு மூலக்கூறுகளான ATP மற்றும் NADH ஆகியவற்றின் தேறிய ஆதாயத்தால் சிறப்பிக்கப்படுகிறது. ஆயத்தக் கட்டத்தில் குளுக்கோஸானது இரண்டு டிரையோஸ் சர்க்கரைகளாகுவதால், பயன்பெறு கட்டத்திலுள்ள ஒவ்வொரு எதிர்வினையும் ஒரு குளுக்கோஸ் மூலக்கூறுக்கு இரண்டு தடவைகள் நிகழும். இதன் விளைவாக 2 NADH மூலக்கூறுகளும், 4 ATP மூலக்கூறுகளும் உருவாகும், எனவே குளுக்கோஸ் ஒன்றுக்குரிய சர்க்கரைச் சிதைவு வழிமுறையிலிருந்து ஆதாயமாக 2 NADH மூலக்கூறுகளும், 2 ATP மூலக்கூறுகளும் கிடைக்கும்.
| NAD+ இன் இரு மூலக்கூறுகளைத் தாழ்த்த ஹைட்ரசன் பயன்படுத்தப்படும். ஹைட்ரசன் அணுச் சமநிலை மற்றும் ஏற்றச் சமநிலை இரண்டும் பேணப்படுகின்றன, ஏனெனில் பாஸ்பேட் (Pi) குழுவானது உண்மையில் ஹைட்ரசன் பாஸ்பேட் எதிரயனி (HPO42-)[3] வடிவில் இருக்கிறது, இது மேலதிக H+ அயனியை வழங்குவதற்கு பிரிகையடைந்து, இரு பக்கத்திலும் தேறிய ஏற்றம் -3 ஐக் கொடுக்கிறது. |
| ||||||||||||||||||||
| இந்தப் படிநிலையானது பாஸ்பேட் குழுவொன்றை பாஸ்போகிளிசரேட்டு கைனேஸ் மூலமாக 1,3-பிஸ்பாஸ்போகிளிசரேட்டிலிருந்து ADP ஆக மாற்றும் நொதிய மாற்றமாகும், ATP மற்றும் 3-பாஸ்போகிளிசரேட்டு உருவாகின்றன. இந்தப் படிநிலையில், சர்க்கரைச் சிதைவானது சரிசமப் புள்ளியை அடைந்துள்ளது: 2 மூலக்கூறுகள் ATP உள்ளெடுக்கப்பட்டன, இப்போது 2 புதிய மூலக்கூறுகள் தொகுக்கப்பட்டுள்ளன. தளப்பொருள்-நிலை பாஸ்ஃபோ ஏற்றப் படிநிலைகள் இரண்டில் ஒன்றான இந்தப் படிநிலைக்கு ADP தேவை; ஆகவேதான், கலத்தில் ஏராளமான ATP (மற்றும் சிறிதளவு ADP) இருக்கும்போது, இந்த வினை நிகழாது. ஏனென்றால், ATP ஆனது வளர்சிதை மாற்றத்துக்கு உள்ளாக்கப்படாதபோது, ஒப்பீட்டளவில் இது விரைவாகச் சிதைவடைகிறது, சர்க்கரைச் சிதைவு வழிமுறையில் இதுவொரு முக்கியமான சீராக்கப் புள்ளியாகும். உண்மையில் ADP ஆனது ADPMg- ஆகவும், ATP ஆனது ATPMg2- ஆகவும் இருக்கின்றன, இரு பக்கங்களிலும் -5 இல் ஏற்றங்களைச் சமப்படுத்துகின்றன.துணைக்காரணிகள்: Mg2+ |
| ||||||||||||||||||||
| பாஸ்போகிளிசரேட்டு மியூட்டேஸ் இப்போது 2-பாஸ்போகிளிசரேட்டை உருவாக்கும். |
| ||||||||||||||||||||
| எனோலேஸ் அடுத்து 2-பாஸ்போகிளிசரேட்டு இலிருந்து பாஸ்போஎனோல்பைருவேட்டை உருவாக்கும்.துணைக்காரணிகள்: 2 Mg2+: கார்பொக்ஸிலேட் குழு தளப்பொருளுடன் ஒழுங்கமைக்க ஒரு "இணக்கமான" அயன், மற்றும் நீரகற்றலில் ஈடுபடும் ஒரு "ஊக்குவிக்கும்" அயன் ஆகும். |
| ||||||||||||||||||||
| இறுதித் தளப்பொருள்-நிலை பாஸ்ஃபோ ஏற்றமானது இப்போது பைருவேட் கைனேஸ் நொதியம் காரணமாக ஒரு மூலக்கூறு பைருவேட் மற்றும் ஒரு மூலக்கூறு ATP ஆகியவற்றை உருவாக்கும். இது பாஸ்போகிளிசரேட்டு கைனேஸ் படிநிலையை ஒத்த, மேலதிக சீராக்க படிநிலையாகச் செயற்படும்.துணைக்காரணிகள்: Mg2+ |
| ||||||||||||||||||||
சீராக்கல்
தொகுசர்க்கரைச் சிதைவு வழிமுறையிலுள்ள சில படிநிலைகளை மெதுவாக்குவதன் மூலம் அல்லது வேகமாக்குவதன் மூலம் சர்க்கரைச் சிதைவு சீராக்கப்படுகிறது. இது சர்க்கரைச் சிதைவில் ஈடுபடுகின்ற நொதியங்களை தடுப்பதன் மூலம் அல்லது செயல்படுத்துவதன் மூலம் அடையப்படுகிறது. ஒவ்வொரு படிநிலைக்குமான கட்டில்லாச் சக்தியில், ΔG உள்ள மாற்றத்தைக் கணிப்பதன் மூலம் சீராக்கப்படுகின்ற படிநிலைகள் தீர்மானிக்கப்படக்கூடும் விளைபொருள்களும், தாக்குபொருள்களும் சமநிலையில் உள்ளன எனில், அந்தப் படிநிலையை சீராக்கத் தேவையில்லை எனக் கருதப்படும். சமநிலையிலுள்ள தொகுதி ஒன்றுக்கான கட்டில்லாச் சக்தியில் ஏற்படும் மாற்றம் சுழியாக இருப்பதால், கட்டில்லாச் சக்தி மாற்றம் சுழியை அண்டி இருக்கும் எந்தவொரு படிநிலையும் சீராக்கப்படமாட்டாது . ஒரு படிநிலை சீராக்கப்படுகிறது எனில், அந்த படிநிலையின் நொதியமானது அதனால் முடிந்தளவு வேகத்துடன் தாக்குபொருள்களை விளைபொருள்களாக மாற்றவில்லை, இதனால் தாக்குபொருள்கள் அதிகரிக்கின்றன, நொதியம் வேகமாக இயக்கப்படுகிறது எனில் தாக்குபொருள்கள் விளைபொருள்களாக மாற்றப்படலாம். எதிர்வினை வெப்பவியக்கவிசைரீதியாக சாதகமானது என்பதால், படிநிலைக்கான கட்டில்லாச் சக்தி மாற்றம் எதிர்மறையாக இருக்கும். கட்டில்லாச் சக்தியிலுள்ள மாற்றம் மிகப்பெரிய எதிர்மறையாக உள்ள ஒரு படிநிலையானது சீராக்கப்பட வேண்டுமெனக் கருதப்படுகிறது.
கட்டில்லாச் சக்தி மாற்றங்கள்
தொகு| எரித்ரோசைடுகள்[6] | |
| சேர்மம் | செறிவு / mM |
|---|---|
| குளுக்கோஸ் | 5.0 |
| குளுக்கோஸ்-6-பாஸ்பேட் | 0.083 |
| ஃபுருக்டோஸ்-6-பாஸ்பேட் | 0.014 |
| ஃபுருக்டோஸ்-1,6-பிஸ்பாஸ்பேட் | 0.031 |
| டைஹைட்ராக்சிஅசட்டோன் பாஸ்பேட் | 0.14 |
| கிளிசரல்டிகைட்-3-பாஸ்பேட் | 0.019 |
| 1,3-பிஸ்பாஸ்போகிளிசரேட்டு | 0.001 |
| 2,3-பிஸ்பாஸ்போகிளிசரேட்டு | 4.0 |
| 3-பாஸ்போகிளிசரேட்டு | 0.12 |
| 2-பாஸ்போகிளிசரேட்டு | 0.03 |
| பாஸ்போஎனோல்பைருவேட் | 0.023 |
| பைருவேட் | 0.051 |
| ATP | 1.85 |
| ADP | 0.14 |
| Pi | 1.0 |
| Colspan=2 |
சர்க்கரைச் சிதைவு வழிமுறையிலுள்ள ஒவ்வொரு படிக்குமான கட்டில்லாச் சக்தியிலுள்ள மாற்றம், ΔG என்பதை ΔG = ΔG °' + RT ln Q ஐப் பயன்படுத்திக் கணிக்கலாம், இங்கே Q என்பது எதிர்வினை ஈவு ஆகும். இதற்காக வளர்சிதை மாற்றத்தில் உருவான பொருள்களின் செறிவுகளை அறியவேண்டும். NAD+ மற்றும் NADH செறிவுகள் தவிர, இரத்தச் சிவப்பணுகளுக்கான இந்த அனைத்து மதிப்புகளும் கிடைக்கின்றன. NAD+, NADH|NAD+, NADH ஆகியவற்றின் விகிதம் அண்ணளவாக 1, இதன்விளைவாக இந்த செறிவுகள் எதிர்வினை ஈவில் சேர்க்கப்படாமல் தவிர்க்கப்படுகின்றன. (எதிர்வினைகளில் எதிரெதிர்ப் பக்கங்களில் NAD+ மற்றும் NADH கிடைப்பதால், ஒன்று பின்னத்தில் மேல் இலக்கமாகவும் அடுத்தது பின்னத்தில் கீழ் இலக்கமாகவும் இருக்கும்.)
ஒவ்வொரு படிநிலையினதும் அளக்கப்பட்ட செறிவுகள் மற்றும் நிலையான கட்டில்லாச் சக்தி மாற்றங்களைப் பயன்படுத்தி உண்மையான கட்டில்லாச் சக்தி மாற்றத்தைக் கணிக்கலாம்.
| [7] | |||
| படிநிலை | எதிர்வினை | ΔG °' / (கி.ஜூ/மோல்) | ΔG / (கி.ஜூ/மோல்) |
|---|---|---|---|
| 1 | குளுக்கோஸ் + ATP4- → குளுக்கோஸ்-6-பாஸ்பேட்2- + ADP3- + H+ | -16.7 | -34 |
| 2 | குளுக்கோஸ்-6-பாஸ்பேட்2- → ஃபுருக்டோஸ்-6-பாஸ்பேட்2- | 1.67 | -2.9 |
| 3 | ஃபுருக்டோஸ்-6-பாஸ்பேட்2- + ATP4- → ஃபுருக்டோஸ்-1,6-பிஸ்பாஸ்பேட்4- + ADP3- + H+ | -14.2 | -19 |
| 4 | ஃபுருக்டோஸ்-1,6-பிஸ்பாஸ்பேட்4- → டைஹைட்ராக்சிஅசட்டோன் பாஸ்பேட்2- + கிளிசரல்டிகைட்-3-பாஸ்பேட்2- | 23.9 | -0.23 |
| 5 | டைஹைட்ராக்சிஅசட்டோன் பாஸ்பேட்2- → கிளிசரல்டிகைட்-3-பாஸ்பேட்2- | 7.56 | 2.4 |
| 6 | கிளிசரல்டிகைட்-3-பாஸ்பேட்2- + Pi2- + NAD+ → 1,3-பிஸ்பாஸ்போகிளிசரேட்டு4- + NADH + H+ | 6.30 | -1.29 |
| 7 | 1,3-பிஸ்பாஸ்போகிளிசரேட்டு4- + ADP3- → 3-பாஸ்போகிளிசரேட்டு3- + ATP4- | -18.9 | 0.09 |
| 8 | 3-பாஸ்போகிளிசரேட்டு3- → 2-பாஸ்போகிளிசரேட்டு3- | 4.4 | 0.83 |
| 9 | 2-பாஸ்போகிளிசரேட்டு3- → பாஸ்போஎனோல்பைருவேட்3- + H2O | 1.8 | 1.1 |
| 10 | பாஸ்போஎனோல்பைருவேட்3- + ADP3- + H+ → பைருவேட்- + ATP4- | -31.7 | -23.0 |
செங்குருதிக் குழியத்திலுள்ள வளர்சிதை மாற்றத்தில் உருவான பொருள்களின் உடற்றொழிலுக்குரிய செறிவுகளை அளப்பதிலிருந்து, அந்த கல வகைக்கு, சர்க்கரைச் சிதைவிலுள்ள கிட்டத்தட்ட ஏழு படிநிலைகள் சமநிலையில் இருப்பது போல தோன்றுகிறது. அவற்றில் மூன்று படிநிலைகள் —மிகப்பெரிய எதிர்மறையான கட்டில்லாச் சக்தி மாற்றங்களுடன் உள்ளவை—சமநிலையில் இல்லை, அவை மீளும் தன்மையற்றவை எனப்படுகின்றன; இதுபோன்ற படிநிலைகள் அடிக்கடி சீராக்கலுக்கு உள்ளாகின்றன.
படத்திலுள்ள படிநிலை 5 பிற படிநிலைகளுக்குப் பின்னால் காண்பிக்கப்படுகிறது, ஏனெனில் அந்த படிநிலை ஒரு பக்க எதிர்வினையாகும், இது இடைநிலையான கிளிசரல்டிகைட்-3-பாஸ்பேட்டின் செறிவைக் குறைக்கலாம் அல்லது கூட்டலாம். அந்தச் சேர்மம் டிரையோஸ் பாஸ்பேட் ஐசோமரேஸ் நொதியத்தால் டைஹைட்ராக்சிஅசட்டோன் பாஸ்பேட்டாக மாற்றப்படுகிறது, இது ஊக்குகின்றரீதியில் சிறந்த நொதியம்; இதன் வீதம் மிகவும் வேகமானது, ஆகவே எதிர்வினை சமநிலையில் இருக்குமெனக் கருதப்படுகிறது. ΔG சுழியில்லை எனும்போது செங்குருதிக் குழியத்திலுள்ள உண்மையான செறிவுகள் சரியாக அறியப்படவில்லை என்பதை உணர்த்துகிறது.
உயிர்வேதியியல் தர்க்கம்
தொகுஒன்றுக்கு மேற்பட்ட சீராக்கல் புள்ளிகள் இருப்பதானது, அந்த புள்ளிகளுக்கிடையிலான இடைநிலைகள் பிற செயல்முறைகள் மூலமாக கிளைகோலைஸிஸ் வழிமுறைக்குள் நுழைந்து வெளியேறுவதைக் குறிப்பிடுகின்றது. எடுத்துக்காட்டாக, முதலாவது சீராக்கல் படிநிலையில், ஹெக்ஸோகைனேஸ் குளுக்கோஸை குளுக்கோஸ்-6-பாஸ்பேட்டாக மாற்றும். சர்க்கரைச் சிதைவு வழிமுறையில் தொடர்வதற்குப் பதிலாக, இந்த இடைநிலையானது கிளைக்கோசன் அல்லது மாவுச்சத்து போன்ற குளுக்கோஸ் சேமிப்பு மூலக்கூறுகளாக மாற்றப்படலாம். பின்னோக்கிய எதிர்வினை, நிறுத்தப்படுகிறது, எ.கா. கிளைக்கோசன் முதன்மையாக குளுக்கோஸ்-6-பாஸ்பேட்டை உருவாக்குகிறது; எதிர்வினையில் மிகக் குறைந்தளவு கட்டில்லா குளுக்கோஸ் உருவாக்கப்படுகிறது. அவ்வாறு உருவாக்கப்பட்ட குளுக்கோஸ்-6-பாஸ்பேட் முதலாவது கட்டுப்பாட்டுப் புள்ளிக்குப் பின்னர் சர்க்கரைச் சிதைவில் நுழையலாம்.
இரண்டாவது சீராக்கல் படிநிலையில் (சர்க்கரைச் சிதைவின் மூன்றாவது படிநிலை) பாஸ்போஃபுருக்டோகைனேஸ் ஃபுருக்டோஸ்-6-பாஸ்பேட்டை ஃபுருக்டோஸ்-1,6-பிஸ் பாஸ்பேட்டாக மாற்றும், இது பின்னர் கிளிசரால்டிகைட்-3-பாஸ்பேட் மற்றும் டைஹைட்ராக்சி அசட்டோன் பாஸ்பேட் ஆகியவையாக மாற்றப்படும். டைஹைட்ராக்சிஅசட்டோன் பாஸ்பேட்டை கிளிசரோல்-3-பாஸ்பேட்டாக மாற்றுவதன் மூலம்ம் சர்க்கரைச் சிதைவிலிருந்து அகற்றலாம், இது ட்ரைகிளிசரைட்டுகள் உருவாக்கப் பயன்படும்.[8] மாறாக, டிரைகிளிசரைடுகளை கொழுப்பமிலங்கள் மற்றும் கிளிசராலாக உடைக்கலாம்; பிந்தையது படிப்படியாக டைஹைட்ராக்சி அசெட்டோன் பாஸ்பேட்டாக மாற்றப்படலாம், இது இரண்டாம் கட்டுப்பாட்டுப் புள்ளியின் பின்னர் சர்க்கரைச் சிதைவில் நுழையும்.
சீராக்கல்
தொகுமூன்று சீராக்கல் நொதியங்கள் ஆவன ஹெக்ஸோகைனேஸ், பாஸ்போஃபுருக்டோகைனேஸ் மற்றும் பைருவேட் கைனேஸ்.
சர்க்கரைச் சிதைவு வழிமுறையினூடான பாயம் கலத்தின் உட்புறம் மற்றும் வெளிப்புறம் இரண்டின் நிலமைகளுக்கு அமையவும் சீராக்கப்படும். ஈரலிலுள்ள வீதமானது முக்கிய கலமுறைத் தேவைகளைப் பூர்த்திசெய்ய சீராக்கப்படும்: (1) ATP உருவாக்கம், (2) உயிரியல் தொகுப்பு ரீதியான எதிர்வினைகளுக்கான கட்டுமானத் தொகுதிகளை வழங்குதல், மற்றும் (3) இரத்த குளுக்கோஸைக் குறைத்தல், இது ஈரலின் முக்கியமான செயல்பாடுகளில் ஒன்று. இரத்தச் சர்க்கரை குறையும்போது, பின்னோக்கிய செயன்முறையான, குளுக்கோசுப் புத்தாக்கத்தை அனுமதிப்பதற்காக, ஈரலில் சர்க்கரைச் சிதைவு நிறுத்தப்படும். சர்க்கரைச் சிதைவில், ஹெக்ஸோகைனேஸ், பாஸ்போஃபுருக்டோகைனேஸ் மற்றும் பைருவேட் கைனேஸ் ஆகியவற்றால் ஊக்குவிக்கப்பட்ட வினைகள் பெரும்பாலான உயிரினங்களில் திறனுள்ள வகையில் மீளும் தன்மையற்றவை. வளர்சிதை மாற்ற வழிமுறைகளில், இந்த நொதியங்கள் கட்டுப்பாட்டுக்குச் சாத்தியமான தளங்களாகும், மேலுள்ள மூன்று நொதியங்களுமே சர்க்கரைச் சிதைவில் இந்த நோக்கத்துக்காகச் செயல்படுகின்றன.
ஹெக்ஸோகைனேஸ்
தொகுவிலங்குகளில், ஈரலால் மேற்கொள்ளப்படும் இரத்தக் குளுக்கோஸ் மட்டங்களின் சீராக்கமானது சீரான உடல் நிலையின் மிக முக்கியமான பாகமாகும். ஈரல் கலங்களில், மேலதிக G6P (குளுக்கோஸ்-6-பாஸ்பேட்) ஆனது கிளைக்கோசனுக்கு மாறுவதற்காக G1P ஆக மாற்றப்படக்கூடும், அல்லது மாறாக சர்க்கரைச் சிதைவினால் அசெட்டைல்-CoA ஆக மாற்றப்பட்டு, பின்னர் சிட்ரேட்டாக மாற்றப்படும். மேலதிக சிட்ரேட் சைடோசாலுக்கு அனுப்பப்படும், அங்கு ATP சிட்ரேட் சிதைப்பியானது அசெட்டைல்-CoA மற்றும் OAA ஐ மீளுருவாக்கம் செய்யும். குளுக்கோசின் செறிவு குருதியில் அதிகமாக உள்ளபோது அவற்றைப் பயன்படுத்தும் முக்கியமான இரு வழிகளான கொழுப்பமிலத் தயாரிப்பு மற்றும் கொலஸ்ட்ரால் தயாரிப்பு ஆகியவற்றில் அசெட்டைல்-CoA பின்னர் பயன்படுத்தப்படும். ஈரலில் ஹெக்ஸோகைனேஸ் மற்றும் குளுக்கோகைனேஸ் ஆகிய இரண்டுமே உள்ளன; பிந்தையது குளுக்கோஸை G6P ஆக பாஸ்ஃபோ ஏற்றம் செய்வதை ஊக்குவிக்கும், G6P ஆல் தடுக்கப்படமாட்டாது. ஆகவே இது ஹெக்ஸோகைனேஸ் செயல்பாடு குறைவாக இருந்தாலும் கூட, குளுக்கோசானது கிளைக்கோஜன், கொழுப்பமிலங்கள் மற்றும் கொலஸ்ட்ரால் ஆகியவையாக மாற்றப்பட அனுமதிக்கும்.[9] குருதி குளுக்கோஸ் மட்டங்கள் அதிகமாக இருக்கும்போது இது மிகவும் முக்கியமானது. இரத்ததசை சர்க்கரைக் குறைவாக இருக்கும்போது, கிளைக்கோஜை மீண்டும் G6P ஆக மாற்ற முடியும், பின்னர் ஈரலுக்கு தனித்துவமான குளுக்கோஸ் 6-பாஸ்பட்டேஸ் நொதியத்தால் குளுக்கோஸாக மாற்றப்படும். உண்ணாவிரதத்தின்போது இரத்த சர்க்கரை மட்டங்களைப் பேணுவதற்கான ஈரலின் பங்களிப்புக்கு இந்த பின்னோக்கிய எதிர்வினை முக்கியமானதாகும். அநேகமான நிலைமைகளின் கீழ் சக்தி மூலமாக குளுக்கோஸை மூளை பயன்படுத்துவதால், இது மூளையின் செயல்பாட்டுக்கு மிக முக்கியமானது.
பாஸ்போஃபுருக்டோகைனேஸ்
தொகுபாஸ்போ ஃபுருக்டோகைனேஸ் என்பது சர்க்கரைச் சிதைவு வழிமுறையில் முக்கியமான ஒரு கட்டுப்பாட்டுப் புள்ளியாகும், ஏனெனில் இது மீளும் தன்மையற்ற படிநிலைகளில் ஒன்று மற்றும் முக்கிய அலொஸ்டெரிக் விளைவாக்கிகளான, AMP மற்றும் ஃபுருக்டோஸ் 2,6-பிஸ் பாஸ்பேட் (F2,6BP) ஆகியவற்றைக் கொண்டுள்ளது.
ஃபுருக்டோஸ் 2,6-பிஸ் பாஸ்பேட் (F2,6BP) பாஸ்போஃபுருக்டோகைனேஸின் (PFK-1) ஆற்றல்மிக்க செயலூக்கியாகும், இது F6P ஐ ஒரு இரண்டாம் பாஸ்போஃபுருக்டோகைனேஸ் (PFK2) பாஸ்போ ஏற்றம் செய்யும்போது தொகுக்கப்படுகிறது. ஈரலில், இரத்தச் சர்க்கரை குறைவாக இருந்து, குளூக்கோகான் cAMP ஐ அதிகரிக்கும்போது, PFK2 ஆனது புரத கைனேஸ் A ஆல் பாஸ்போ ஏற்றம் செய்யப்படும். பாஸ்ஃபோ ஏற்றம் PFK2 ஐச் செயலற்றதாக்கும், தோடு இந்த புரதத்திலுள்ள இன்னொரு களம் ஃபுருக்டோஸ் 2,6-பிஸ்பாஸ்பட்டேஸாக செயல்படுத்தப்படும், இது F2,6BP ஐ மீண்டும் F6P ஆக மாற்றும். குளூக்கோகான் மற்றும் எப்பிநெப்பிரின் இரண்டும் ஈரலில் உயர் மட்ட cAMP ஐ உண்டாக்கும். ஈரலில் குறைவான ஃபுருக்டோஸ்-2,6-பிஸ்பாஸ்பேட் மட்டங்களின் விளைவால் பாஸ்போஃபுருக்டோகைனேஸ் செயல்பாடு குறைகிறது, ஃபுருக்டோஸ் 1,6-பிஸ்பாஸ்பட்டேஸ் செயல்பாடு அதிகரிக்கிறது, ஆகவே குளுக்கோசுப்புத்தாக்கம் (அடிப்படையில் "பின்னோக்கிய சர்க்கரைச் சிதைவு") சாதகமாகிறது. இந்த ஓமோன்களுக்கு ஈரலின் பதிலளிப்பாக இரத்தத்தில் குளுக்கோஸ் விடுவிக்கப்படுவதால், இதுபோன்ற நிலமைகளில் ஈரலில் பங்களிப்புடன் இது ஒருசீரானது.
ATP ஆனது PFK நொதியத்திலுள்ள அலொஸ்டெரிக் விளைவாக்கிக்காக AMP உடன் போட்டிபோடுகிறது. கலங்களிலுள்ள ATP செறிவுகள் AMP ஐ மிக அதிகளவானவை, பொதுவாக 100-மடங்கு உயர்வானவை,[10] ஆனால் உடற்தொழிலுக்குரிய நிலமைகளின்கீழ், ATP செறிவு கிட்டத்தட்ட 10% ஐவிட அதிகமாக மாறமாட்டாது, ஆனால் ATP இல் 10% வீழ்ச்சியானது AMP இல் 6-மடங்கு அதிகரிப்பை ஏற்படுத்தும்.[11] ஆகவே, அலொஸ்டெரிக் விளைவாக்கியாக ATP இன் தொடர்பு கேள்விக்குரியது. AMP இல் ஏற்படும் அதிகரிப்பு கலத்தில் ஏற்படும் சக்தி ஏற்றத்திலுள்ள வீழ்ச்சியின் பின்விளைவாகும்.
ஆய்வுகூடச் சோதனையில் ATP இன் தடுக்கும் விளைவை அதிகரிப்பதன் மூலம் சோதனைசெய்தபோது, சிட்ரேட் பாஸ்போஃபுருக்டோகைனேஸைத் தடுக்கிறது. இருந்தபோதிலும், இது உயிரியல் செயல்முறை யில் அர்த்தமுள்ள விளைவைத் தருமா என்பது சந்தேகமே, ஏனெனில் சைடோசாலிலுள்ள சிட்ரேட் பிரதானமாக கொழுப்பமிலம் மற்றும் கொலஸ்ட்ரால் தொகுப்புக்காக அசெட்டைல்-CoA க்கு மாற்றுவதற்கே பயன்படுத்தப்படும்.
பைருவேட் கைனேஸ்
தொகுஇந்த நொதியம் சர்க்கரைச் சிதைவின் கடைசிப் படிநிலையை ஊக்குகிறது, இதில் பைருவேட்டும் ATP உம் உருவாக்கப்படுகின்றன. இந்த நொதியத்தின் சீராக்கல் முக்கிய தலைப்பான, பைருவேட் கைனேஸில் விவாதிக்கப்படுகிறது.
சர்க்கரைச் சிதைவிற்கு பிந்திய செயல்முறைகள்
தொகுசர்க்கரைச் சிதைவின் ஒட்டுமொத்த செயல்முறையாவது:
- குளுக்கோஸ் + 2 NAD+ + 2 ADP + 2 Pi → 2 பைருவேட் + 2 NADH + 2 H+ + 2 ATP + 2 H2O
சர்க்கரைச் சிதைவு முடிவிலியாக தொடர்ந்தால், அனைத்து NAD+ உம் பயன்படுத்தப்பட்டுவிடலாம், ஆகவே சர்க்கரைச் சிதைவு நிறுத்தப்படலாம். சர்க்கரைச் சிதைவு தொடர்வதை அனுமதிக்க, உயிரங்கிகள் கட்டாயமாக NADH ஐ மீண்டும் NAD+ ஆக உயிர்வளியேற்றக்கூடியதாக இருக்கவேண்டும்.
காற்றின்றிவாழ் சுவாசம்
தொகுஇதைச் செய்யும் ஒரு செய்முறை என்னவென்றால் எளிதாக பைருவேட்டை உயிர்வளியேற்றம் செய்வதாகும்; இந்த செயல்முறையில் பைருவேட்டானது, லேக்டிக் அமிலம் நொதித்தல் என்றழைக்கப்படும் ஒரு செயல்முறையில் லேக்டேட்டாக மாற்றப்படும்:
- பைருவேட் + NADH + H+ → lactate + NAD+
இந்த செயல்முறையானது தயிர் தயாரிப்பில் ஈடுபடுகின்ற பாக்டீரியாவில் நிகழ்கிறது (லேக்டிக் அமிலம் பாலை கெட்டியாக உறையச் செய்கிறது). உயிர்வளி குறைவான (அல்லது பகுதி-காற்றின்றிவாழ்) நிலைமைகளில், இந்த செயல்முறையானது விலங்குகளிலும்கூட நிகழ்கிறது, எடுத்துக்காட்டாக, உயிர்வளி தீர்ந்துபோன அளவுக்கதிகமாக வேலைசெய்த தசைகள் அல்லது அழிந்துபோன இருதய தசைக் கலங்கள். பல இழையங்களில், இது சக்தியை எடுக்கும் இறுதிக் கலமுறை இடமாகும்; பெரும்பாலான விலங்குகள் நீட்டிக்கப்பட்ட காலத்துக்கு காற்றின்றிய சுவாசத்தைப் பேண முடியாதவை.
ஈஸ்ட் போன்ற சில உயிரங்கிகள், எதனோல் நொதித்தல் எனப்படுகின்ற ஒரு செயன்முறையில் NADH ஐ மீண்டும் NAD+ ஆக மாற்றும். இந்த செயன்முறையில், பைருவேட் முதலில் அசெட்டால்டிஹைட் மற்றும் கார்பனீரொக்சைட்டாக மாற்றப்பட்டு பின்னர் எதனோலாக மாற்றப்படும்.
லேக்டிக் அமிலம் நொதித்தல் மற்றும் எதனோல் நொதித்தல் ஆகியவை உயிர்வளி இல்லாத நிலைமைகளில் நிகழக்கூடியன. இந்த காற்றின்றிவாழ் நொதித்தலானது தமது ஒரேயொரு சக்தி மூலமாக சர்க்கரைச் சிதைவைப் பயன்படுத்த பல தனிக்கல உயிரங்கிகளை அனுமதிக்கிறது.
மேலுள்ள நொதித்தல் எடுத்துக்காட்டுகள் இரண்டிலும், NADH இரண்டு இலத்திரன்களை பைருவேட்டுக்கு இடமாற்றுவதன் மூலம் ஆக்ஸிஜனேற்றப்படுகின்றது.. இருந்தபோதிலும், கலமுறை சுவாசத்தில், முனை இலத்திரன் ஏற்பிகளாக பலவகைப்பட்ட சேர்மங்களை காற்றின்றிவாழ் பாக்டீரியாக்கள் பயன்படுத்துகின்றன:நைட்ரேட்டுகள் மற்றும் நைட்ரைட்டுகள் போன்ற நைட்ரசன் அடங்கிய சேர்மங்கள்; சல்பேட்டுகள், சல்பைட்டுகள், கந்தக ஈரொக்சைட்டு மற்றும் அடிப்படை கந்தகம் போன்ற கந்தக சேர்மங்கள்; கார்பனீரொக்சைட்டு; இரும்புச் சேர்மங்கள்; மங்கனீஸ் சேர்மங்கள்; கோபால்ட் சேர்மங்கள்; மற்றும் யுரேனியம் சேர்மங்கள்.
காற்றுவாழ் சுவாசம்
தொகுகாற்றுவாழ் உயிரங்கிகளில், சுவாசத்தின் இறுதி இலத்திரன் ஏற்பியாக காற்றிலுள்ள உயிர்வளியைப் பயன்படுத்த சிக்கலான பொறிமுறை உருவாகியுள்ளது.
- முதலில், இழைமணிகளில் பைருவேட் கார்பாக்சைல்நீக்கம் என அழைக்கப்படும் செயன்முறையில் பைருவேட்டானது அசெட்டைல்-CoA மற்றும் CO2 ஆகியனவாக மாற்றப்படும்.
- இரண்டாவதாக, அசெட்டைல்-CoA ஆனது சிட்ரிக் அமில வட்டத்தில் நுழைகிறது, இங்கே இது காபனீரொக்சைட்டு மற்றும் நீர் ஆகியனவாக பூரண உயிர்வளியேற்றம் நடந்து இன்னும் அதிகமாக NADH உருவாகும்.
- மூன்றாவது, இறுதி இலத்திரன் ஏற்பியாக உயிர்வளியைப் பயன்படுத்தி இலத்திரன் இடமாற்ற சங்கிலி மூலமாக, NADH ஆனது NAD+ ஆக உயிர்வளியேற்றப்படுகிறது. இந்த செயன்முறை இழைமணியின் உள் மென்படலம் வழியே "ஹைட்ரசன் அயன் சாய்வை" உருவாக்கும்.
- ஆக்சியேற்ற பாஸ்ஃபோ ஏற்றம் எனப்படுகின்ற செயன்முறையில் பெருமளவான ATP ஐ உருவாக்க புரோட்டான் சாய்வு பயன்படுத்தப்படும்.
பிற வழிமுறைகளுக்கான இடைநிலைகள்
தொகுகுளுக்கோஸை பைருவேட்டாக உயிர்வளியேற்றம் செய்யும்போது, சாத்தியமான இரசாயன சக்தியை பயன்படுத்தக்கூடிய இரசாயன சக்தியாக மாற்றுவதுடன் தொடர்பாக, சர்க்கரைச் சிதைவின் அழிக்கும் பங்கு பற்றியே இந்த கட்டுரை கவனமெடுக்கிறது. இருந்தபோதிலும், சர்க்கரைச் சிதைவு வழிமுறையிலுள்ள வளர்சிதை மாற்றத்தில் உருவான பொருள்களில் பலவும்கூட உட்சேர்க்கைக்குரிய வழிமுறைகளால் பயன்படுத்தப்படுகின்றன, மேலும் இதன் விளைவாக, உயிரியல் தொகுப்புக்கான கார்பன் கட்டமைப்புகள் வழங்கலைப் பேணுவதற்கு வழிமுறையூடான பாய்மம் முக்கியமானது.
மேலும், வழிமுறையில் உட்செல்லும் அனைத்து கார்பன்களும் பைருவேட்டாக வெளியேறுவதில்லை, பிற வழிமுறைகளுக்கான கார்பன் சேர்மங்களை வழங்குவதற்கு முந்தைய நிலைகளில் வெறியேற்றப்படக்கூடும்.
இந்த வளர்சிதை மாற்ற வழிமுறைகள் அனைத்தும், வளர்சிதை மாற்றத்தில் உருவான பொருள்களின் மூலமாக கண்டிப்பாக கிளைகோலைஸிஸில் தங்கியிருக்கும்:
- குளுக்கோசுப்புத்தாக்கம்
- கொழுப்பு வளர்சிதை மாற்றம்
- பெண்டோஸ் பாஸ்பேட் வழிமுறை
- சிட்ரிக் அமில சுழற்சி, இது பின்வருவனவற்றுக்கு வழிவகுக்கும்:
-
- அமினோ அமிலத் தொகுப்பு
- நியூக்ளியோடைட்டு தொகுப்பு
- டெட்ராபைர்ரோல் தொகுப்பு
உட்சேர்க்கைக்குரிய வளர்சிதை மாற்றத் தோற்றத்திலிருந்து, தொகுப்பு எதிர்வினைகளை நடத்துவதில் NADH பங்களிக்கிறது, இவ்வாறு செய்வதால் கலத்திலுள்ள NADP+ சேமிப்பை NADPH ஆக நேரடியாக அல்லது மறைமுகமாக தாழ்த்துகிறது, கலத்தில் உயிரியல் தொகுப்பு வழிமுறைகளுக்கான இன்னொரு முக்கிய தாழ்த்தும்பொருள் இதுவாகும்.
நோயில் சர்க்கரைச் சிதைவு
தொகுமரபுவழி நோய்கள்
தொகுவளர்சிதை மாற்ற வழிமுறையின் முக்கியத்துவம் காரணமாக சர்க்கரைச் சிதைவு மாற்றங்கள் பொதுவாக அரிதானவை, அதாவது நிகழ்கின்ற மாற்றங்களில் பெரும்பாலானவை கலத்தை சுவாசிக்கும் திறனற்றவையாக ஆக்கும், இதனால் ஆரம்ப நிலையிலேயே கல இறப்பு ஏற்படும். இருந்தபோதும், சில மாற்றங்கள் காணப்படுகின்றன.
புற்று நோய்
தொகுகொடிய வேகமாக-வளருகின்ற கட்டிக் கலங்கள், இவை அவற்றின் சாதாரண தோற்ற இழையத்தின் சர்க்கரைச் சிதைவு வீதங்களைவிட பொதுவாக 200 மடங்கு அதிகமான வீதத்தைக் கொண்டிருக்கும். சாதாரணமாக இரண்டு விளக்கங்கள் உள்ளன. ஏற்றுக்கொள்ளப்பட்ட விளக்கம் என்னவென்றால், கட்டிகளுக்கு குறைவான குருதி விநியோகம் உள்ளது, இது அக உயிர்வளியைக் குறைக்கிறது. அளவுக்கதிகமாக வெளிக்காட்டப்பட்ட இழைமணிரீதியாக-கட்டப்பட்டஹெக்ஸோகைனேஸ் வடிவத்துக்கு, இந்த உயர் காற்றுவாழ் சர்க்கரைச் சிதைவு வீதங்கள் சில வழங்கப்படுவதாகவும் சான்று உள்ளது. இந்த இயல்பானது முதன்முதலில் 1930 இல் ஒட்டோ வார்பர்க்கால் விவரிக்கப்பட்டது, ஆகவே இது வார்பர்க் விளைவு எனக் குறிப்பிடப்படுகிறது. கலங்களின் கட்டுப்படுத்தப்படாத வளர்ச்சி காரணமாக அன்றி, முதன்மையாக வளர்சிதை மாற்றத்தில் செயல்பாடு குழப்பம் ஏற்படுவதன் காரணமாக புற்றுநோய் ஏற்படுவதாக வார்பர்க் கருதுகோள் கூறுகிறது. இழைமணிக்குரிய வளர்சிதை மாற்றத்தைப் பாதிக்கவும், கீட்டோஜீனிக் உணவு உள்ளடங்கலாக பல வழிகளில் புற்றுநோய்க் கலங்களை பட்டினிபோடச் செய்வதன் மூலம் புற்றுநோய்க்கு சிகிச்சை அளிக்கவும் ஆராய்ச்சிகள் நடந்துவருகின்றன.
இந்த உயர் சர்க்கரைச் சிதைவு வீதமானது முக்கிய மருத்துவ பயன்பாடுகளை உடையது, ஏனெனில் 2-18F-2-டீஆக்ஸிகுளுக்கோஸ்|2-18F-2-டீஆக்ஸிகுளுக்கோஸ் (FDG) (கதிரியக்கம் மூலம் மாற்றப்பட்ட ஹெக்ஸோகைனேஸ் தளப்பொருள்) உள்ளெடுக்கப்படுதலை பாசிட்ரான் உமிழ்வு கதிர் வீச்சு வரைவுடன் (PET) படமாக்கல் மூலமாக புற்றுநோய்களை மருத்துவரீதியாகக் கண்டுபிடிக்கவும், சிகிச்சைக்கான விளைவுகளைக் கண்காணிக்கவும் கொடிய கட்டிகளின் மூலமான உயர் காற்றுவாழ் சர்க்கரைச் சிதைவு பயன்படுத்தப்படுகிறது.[12][13]
அல்சைமர் நோய்கள்
தொகுசெயல்பாடு குழப்பமடைந்த சர்க்கரைச் சிதைவு அல்லது முன்-பாக்க-பக்கத்தில் குளுக்கோஸ் வளர்சிதை மாற்றம் மைய(cingulate) மேற்பட்டைகள் என்பது அல்சைமர் நோயு [14] தொடர்பானது, இது பெரும்பாலும் மூளை முதுகுத்தண்டு பாயத்தில் (CSF) [15] குறைக்கப்பட்ட அமைலொய்ட் β (1-42) (Aβ42) மற்றும் அதிகரிக்கப்பட்ட tau, பாஸ்போ ஏற்றப்பட்ட tau இன் காரணமாக ஏற்படும்
மாற்றுப் பெயரீட்டுமுறை
தொகுசர்க்கரைச் சிதைவிலுள்ள சில வளர்சிதை மாற்றத்தில் உருவான பொருள்களுக்கு மாற்று பெயர்களும், பெயரீடுகளும் உள்ளன. ஏனெனில், இவற்றில் சில கால்வன் வட்டம் போன்ற பிற வழிமுறைகளுக்கும் பொதுவானவை என்பதாலாகும்.
| இந்தக் கட்டுரை | மாற்றுப் பெயர்கள் | மாற்றுப் பெயரீடுகள் | ||
|---|---|---|---|---|
| 1 | குளுக்கோஸ் | Glc | டெக்ஸ்ட்ராஸ் | |
| 3 | ஃபுருக்டோஸ் 6-பாஸ்பேட் | F6P | ||
| 4 | ஃபுருக்டோஸ் 1,6-பிஸ்பாஸ்பேட் | F1,6BP | ஃபுருக்டோஸ் 1,6-டைபாஸ்பேட் | FBP , FDP , F1,6DP |
| 5 | டைஹைட்ராக்சிஅசட்டோன் பாஸ்பேட் | DHAP | கிளிசெரோன் பாஸ்பேட் | |
| 6 | கிளிசரல்டிகைட் 3-பாஸ்பேட் | GADP | 3-பாஸ்போகிளிசரல்டிகைட் | PGAL , G3P , GALP ,GAP ,TP |
| 7 | 1,3-பிஸ்பாஸ்போகிளிசரேட்டு | 1,3BPG | கிளிசரேட்டு 1,3-பிஸ்பாஸ்பேட், கிளிசரேட்டு 1,3-diபாஸ்பேட், 1,3-டைபாஸ்போகிளிசரேட்டு |
PGAP , BPG , DPG |
| 8 | 3-பாஸ்போகிளிசரேட்டு | 3PG | கிளிசரேட்டு 3-பாஸ்பேட் | PGA , GP |
| 9 | 2-பாஸ்போகிளிசரேட்டு | 2PG | கிளிசரேட்டு 2-பாஸ்பேட் | |
| 10 | பாஸ்போஎனோல்பைருவேட் | PEP | ||
| 11 | பைருவேட் | Pyr | பைரூவிக் அமிலம் | |
குறிப்புகள்
தொகு- ↑ வெப்ஸ்டர்ஸ் நியூ இண்டர்நேஷனல் டிக்சனரி ஆஃப் தி இங்கிலிஷ் லாங்வேஜ், 2ஆம் பதி. (1937) மெர்ரியன் கம்பனி, ஸ்பிரிங்ஃபீல்ட், மாஸ்.
- ↑ ரோமனோ ஏ.ஹெச், கன்வே டி. (1996) எவலூசன் ஆஃப் கார்போஹைட்ரேட்டு மெட்டாபோலிக் பாத்வேய்ஸ். ரெஸ் மைக்ரோபியல். 147(6-7):448-55 PubMed
- ↑ 3.0 3.1 எஆசு:10.1007/s11306-008-0142-2
This citation will be automatically completed in the next few minutes. You can jump the queue or expand by hand - ↑ Reeves, R. E.; South D. J., Blytt H. J. and Warren L. G. (1974). "Pyrophosphate: D-fructose 6-phosphate 1-phosphotransferase. A new enzyme with the glycolytic function 6-phosphate 1-phosphotransferase". J Biol Chem 249 (24): 7737–7741. பப்மெட்:4372217.
- ↑ Selig, M.; Xavier K. B., Santos H. and Schönheit P. (1997). "Comparative analysis of Embden-Meyerhof and Entner-Doudoroff glycolytic pathways in hyperthermophilic archaea and the bacterium Thermotoga". Arch Microbiol 167 (4): 217–232. பப்மெட்:9075622.
- ↑ Garrett, R.; Grisham, C. M. (2005). Biochemistry (3rd ed.). Belmont, CA: Thomson Brooks/Cole. p. 584. பன்னாட்டுத் தரப்புத்தக எண் 0-534-49011-6.
{{cite book}}: Check|isbn=value: checksum (help) - ↑ Garrett, R.; Grisham, C. M. (2005). Biochemistry (3rd ed.). Belmont, CA: Thomson Brooks/Cole. pp. 582–583. பன்னாட்டுத் தரப்புத்தக எண் 0-534-49011-6.
{{cite book}}: Check|isbn=value: checksum (help) - ↑ Berg, J. M.; Tymoczko, J. L.; Stryer, L. (2007). Biochemistry (6th ed.). New York: Freeman. p. 622. பன்னாட்டுத் தரப்புத்தக எண் 0-534-49011-6.
{{cite book}}: Check|isbn=value: checksum (help) - ↑ வோயட் டி., மற்றும் வோயட் ஜே. ஜி. (2004). உயிரி வேதியியல் 3வது பதிப்பு (நியூ யார்க், ஜான் விலே மற்றும் சன்ஸ், இங்க்.)
- ↑ பெய்ஸ் ஐ., மற்றும் நியூஸ்ஹோல்ம் ஈ. ஏ. (1975). தி கண்டெண்ட்ஸ் ஆஃப் அடினைன் நியுக்ளியோடைட்ஸ், பாஸ்பேஜன்ஸ் அண்ட் சம் கிளைக்கோலிடிக் இண்டர்மீடியேட்ஸ் இன் ரெஸ்டிங் மஸிள்ஸ் ஃப்ரம் வெர்டிபிரேட்ஸ் அண்ட் இன்வெர்டிபிரேட்ஸ். பயோகெம் ஜே 152, 23-32.
- ↑ வோயட் டி., மற்றும் வோயட் ஜே. ஜி. (2004). உயிரிவேதியல் 3வது பதிப்பு (நியூ யார்க், ஜான் விலே மற்றும் சன்ஸ், இங்க்.).
- ↑ "PET Scan: PET Scan Info Reveals ..." பார்க்கப்பட்ட நாள் December 5, 2005.
{{cite web}}: Unknown parameter|dateformat=ignored (help) - ↑ "4320139 549..559" (PDF). பார்க்கப்பட்ட நாள் December 5, 2005.
{{cite web}}: Unknown parameter|dateformat=ignored (help) - ↑ Hunt, A . et al.; Schonknecht, P; Henze, M; Seidl, U; Haberkorn, U; Schroder, J (2007). "Reduced cerebral glucose metabolism in patients at risk for Alzheimer's disease". Psychiatry Research: Neuroimaging 155 (2): 147–154. doi:10.1016/j.pscychresns.2006.12.003.
- ↑ Hunt, A . et al.; Van Der Flier, WM; Blankenstein, MA; Bouwman, FH; Van Kamp, GJ; Barkhof, F; Scheltens, P (2008). "CSF and MRI markers independently contribute to the diagnosis of Alzheimer's disease". Neurobiology of Aging 29 (5): 669–675. doi:10.1016/j.neurobiolaging.2006.11.018. பப்மெட்:17208336. https://archive.org/details/sim_neurobiology-of-aging_2008-05_29_5/page/669.
புற இணைப்புகள்
தொகு- A simplified glycolysis animation பரணிடப்பட்டது 2009-09-04 at the வந்தவழி இயந்திரம் (Adobe Flash required)
- A Detailed Glycolysis Animation provided by IUBMB (Adobe Flash தேவை)
- In protein data bank the glycolytic enzymes in glycolysis பரணிடப்பட்டது 2005-12-21 at the வந்தவழி இயந்திரம்
- In wdv.com cycle with animations
- In biochemweb.org metabolism, Cellular respiration and photosynthesis - The virtual library of biochemistry and cell biology பரணிடப்பட்டது 2005-03-16 at the வந்தவழி இயந்திரம்
- In rahulgladwin.com Notes on glycolysis பரணிடப்பட்டது 2008-06-11 at the வந்தவழி இயந்திரம்
- In ufp.pt The chemical logic behind glycolysis பரணிடப்பட்டது 2013-03-22 at the வந்தவழி இயந்திரம்
- ExPASy இல் expasy biochemical pathways poster