அசிட்டோன்
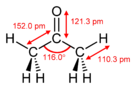
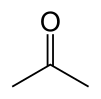
அசிட்டோன் (Acetone) என்பது C3H6O அல்லது (CH3)2CO என்ற மூலக்கூற்று வாய்ப்பாடு கொண்ட ஒரு கரிம வேதியியல் சேர்மமாகும். புரோப்பனோன் என்ற பெயராலும் இதை அழைக்கிறார்கள். இது நிறமற்றதாகவும், எளிதில் ஆவியாகக் கூடியதுமாக காணப்படுகிறது. அசிட்டோன் தீப்பற்றக் கூடிய ஒரு நீர்மமாகவும் உள்ளது. கீட்டோன்கள் வரிசையில் மிகவும் எளிய கீட்டோன் அசிட்டோன் ஆகும்.
| |||
| |||
| பெயர்கள் | |||
|---|---|---|---|
| முறையான ஐயூபிஏசி பெயர்
புரோப்பேன்-2-ஓன்[5] | |||
| வேறு பெயர்கள் | |||
| இனங்காட்டிகள் | |||
| 67-64-1 | |||
| 3DMet | B00058 | ||
| Abbreviations | DMK | ||
Beilstein Reference
|
635680 | ||
| ChEBI | CHEBI:15347 | ||
| ChEMBL | ChEMBL14253 | ||
| ChemSpider | 175 | ||
| EC number | 200-662-2 | ||
Gmelin Reference
|
1466 | ||
| யேமல் -3D படிமங்கள் | Image | ||
| KEGG | D02311 | ||
| ம.பா.த | Acetone | ||
| பப்கெம் | 180 | ||
| வே.ந.வி.ப எண் | AL3150000 | ||
| |||
| UNII | 1364PS73AF | ||
| UN number | 1090 | ||
| பண்புகள் | |||
| C3H6O | |||
| வாய்ப்பாட்டு எடை | 58.08 g·mol−1 | ||
| தோற்றம் | வண்ணமற்ற திரவம் | ||
| மணம் | நெடியுள்ள, எரிச்சலூட்டும், பூவுக்குரிய வாசனையுள்ள திரவம் | ||
| அடர்த்தி | 0.791 கி செ,மீ−3[6] | ||
| காடித்தன்மை எண் (pKa) | 24.2 | ||
| காரத்தன்மை எண் (pKb) | -10.2 | ||
| ஒளிவிலகல் சுட்டெண் (nD) | 1.35900 | ||
| பிசுக்குமை | 0.3075 cP | ||
| கட்டமைப்பு | |||
| மூலக்கூறு வடிவம் | |||
| இருமுனைத் திருப்புமை (Dipole moment) | 2.91 D | ||
| வெப்பவேதியியல் | |||
| Std enthalpy of formation ΔfH |
-250.03-(-248.77) கியூ மோல்−1 | ||
| Std enthalpy of combustion ΔcH |
-1.772 மெகாயூல் மோல்−1 | ||
| நியம மோலார் எந்திரோப்பி S |
200.4 யூ கெ−1 மோல்−1 | ||
| வெப்பக் கொண்மை, C | 125.45 யூ கெ−1 மோல்−1 | ||
| தீங்குகள் | |||
| GHS pictograms |  
| ||
| GHS signal word | அபாயம் | ||
| H225, H319, H336 | |||
| P210, P261, P305+351+338 | |||
| ஈயூ வகைப்பாடு | |||
| R-சொற்றொடர்கள் | R11, R36, R66, R67 | ||
| S-சொற்றொடர்கள் | (S2), S9, S16, S26 | ||
| தீப்பற்றும் வெப்பநிலை | −17 °செ | ||
Threshold Limit Value
|
500 மில்லியனுக்கு பகுதிகள் (TWA), 750 மில்லியனுக்கு பகுதிகள் (STEL) | ||
| Lethal dose or concentration (LD, LC): | |||
LD50 (Median dose)
|
>2000 மி.கி/கி.கி, வாய்வழி (எலி) | ||
| தொடர்புடைய சேர்மங்கள் | |||
| தொடர்புடைய சேர்மங்கள் | பியூடனோன் ஐசோபுரோபனோல் | ||
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |||
அசிட்டோன் தண்ணீருடன் கலக்கிறது. தானே ஒரு கரைப்பானாகவும் செயல்படுகிறது. செட்டோனானது தண்ணீருடன் பிணைக்கப்பட்டு, அதன் சொந்த உரிமையில் ஒரு முக்கிய கரைப்பான், பொதுவாக ஆய்வகங்களில் துப்புறவு பணிகளுக்காக பயன்படுத்தப்படுகிறது. 2010 ஆம் ஆண்டில் மட்டும் உலகம் முழுவதும் 6.7 மில்லியன் டன்கள் அசிட்டோன் உற்பத்தி செய்யப்பட்டது. ஒரு கரைப்பானாகவும், மெத்தில் மெத்தக்ரைலேட்டு மற்றும் பிசுபீனால் ஏ தயாரிக்கவும் மட்டுமே மொத்த அசிட்டோனும் பயன்படுத்தப்பட்டது [7][8]. கரிம வேதியியலில் பொதுவான கட்டுறுப்பு தொகுதியாக அசிட்டோன் பயன்படுகிறது. வீட்டு உபயோகத்தில் சாதாரணமாக, நகச்சாயம் அகற்றியாகவும், சாய மெலிவூட்டியாகவும் பயன்படுகிறது. பலவித கரிமச்சேர்மங்களை உருவாக்கவும் அசிட்டோன் பயன்படுத்தப்படுகிறது.
சாதாரண வளர்சிதை மாற்ற வழிமுறைகளால் அசிட்டோன் மனித உடலில் உற்பத்தி செய்யப்படுகிறது மற்றும் நீக்கவும்படுகிறது. இது பொதுவாக இரத்த மற்றும் சிறுநீரில் உள்ளது. நீரிழிவு நோயால் பாதிக்கப்பட்டவர்கள் பெரிய அளவில் அதை உற்பத்தி செய்கின்றனர். இது இனப்பெருக்க பிரச்சனைகளைக் குறைக்கக்கூடிய சாத்தியக்கூறுகளை மிகக்குறைவாகக் கொண்டுள்ளதாக இனப்பெருக்க நச்சுத்தன்மை சோதனை முடிவுகள் தெரிவிக்கின்றன. இரத்தத்தில் அசிட்டோன், β- ஐதராக்சி பியூட்டரிக் அமிலம், அசிட்டோ அசிட்டிக் அமிலம் போன்ற கீட்டோன்களை அதிகரிக்கச் செய்யும் கீட்டோனாக்க உணவுகள் குழந்தைகளுக்கு உண்டாகும் வலிப்பு நோய்களுக்கு எதிராக செயல்படுகின்றன. கட்டுப்படுத்த முடியாத வலிப்பு நோய்க்கு ஆட்பட்ட குழந்தைகளுக்கும் வலிப்பைக் கட்டுபடுத்த இவை உதவுகின்றன.
வரலாறு
தொகுஅசிட்டோன் முதன் முதலில் இரசவாதிகளால் பின் மத்திய காலத்தில் உற்பத்தி செய்யப்பட்டது. ஈய அசிட்டேட்டு போன்ற உலோக அசிட்டேட்டுகளை இவர்கள் உலர் காய்ச்சி வடித்தல் செய்து அசிட்டோனை தயாரித்தார்கள் [9].
1832 ஆம் ஆண்டு பிரெஞ்சு வேதியியலாளர் யீன் பாப்டிசுட்டு தூமாசு மற்றும் செருமானிய வேதியியலாளர் யசுட்டசு வோன் லைபிக் ஆகியோர் அசிட்டோன்ய்க்கான அனுபவ வாய்ப்பாட்டை உறுதி செய்தனர் [10][11]. 1833 ஆம் ஆண்டு மற்றொரு பிரெஞ்சு வேதியியல் அறிஞரான அண்டோயின் பிசி இதற்கு அசிட்டோன் எனப் பெயரிட்டார். தொடர்புடைய அமிலத்தின் பெயரில் இருந்த வேர் சொல்லுடன் ஒன் என்ற விகுதியைச் சேர்த்துக் கொண்டார். இதன்படி அசிட்டிக் அமிலம் என்ற தொடர்புடைய அமிலத்தின் வேர்ச் சொல்லான அசிட்டிக் உடன் ஓன் என்ற விகுதியைச் சேர்த்து அசிட்டோன் என்று பெயரிட்டார் [12]. 1852 இல் இங்கிலாந்து வேதியியல் அறிஞரான அலெக்சாண்டர் வில்லியம் வில்லியாம்சன் அசிட்டோன் என்பது மெத்தில் அசிட்டைல் என்பதை தெளிவுபடுத்தினார் ;[13]. அடுத்த ஆண்டில் பிரெஞ்சு நாட்டைச் சேர்ந்த வேதியியலர் சார்லசு பிரடெரிக் கெர்கார்டு இதை ஏற்றுக் கொண்டார் [14]. செருமானிய வேதியியலர் ஆகத்து கெக்குலே அசிட்டோனுக்கான கட்டமைப்பு வாய்ப்பாட்டை வெளியிட்டார் [15][16]. 1861 இல் அசிட்டோனுக்கான கட்டமைப்பை யோகான் யோசப் லோசிமிட்டு முன்வைத்தார் [17]. தனியராக வெளியிட்ட காரணத்தினால் அந்த கட்டமைப்பு எவர் கவனத்தையும் ஈர்க்கவில்லை. முதலாம் உலகப் போர் காலத்தில் செய்ம் வெய்சுமான் அசிட்டோன் தயாரிக்கும் முறை ஒன்றை உருவாக்கி செயல்படுத்தினார் [18] .
உயிரியல் தொகுப்பு
தொகுசிறிய அளவு அசிட்டோன் உடலில் உள்ள கீட்டோன் பொருள்களின் கார்பாக்சிலேற்ற நீக்க வினையின் மூலம் உற்பத்தி செய்யப்படுகிறது. நீடித்த உண்ணாவிரதம் மற்றும் உயர் கொழுப்பும் குறைந்த கார்போவைதரேட்டும் உள்ள உணவு எடுத்துக் கொள்ளுதல் போன்ற உணவுப் பழக்கங்கள் கீட்டோசிசை உற்பத்தி செய்கின்றன. உடல் திசுக்களில் உள்ள இவற்றில் அசிட்டோன் உருவாகிறது. குடிப்பழக்கம், நீரிழிவு நோய் போன்ற உடல் நிபந்தனைகள் கீட்டோஅசிடோசிசை உருவாக்குகின்றன. கட்டுபடுத்தமுடியாத கீட்டோசிசு காரணமாக மோசமான விளைவுகளை சந்திக்க நேர்கிறது. இரத்தத்தில் அமிலத் தன்மை அதிகரிக்கிறது.
அசிட்டோன் வளர்சிதைமாற்றத்தின் பயன்
தொகுஅசிட்டோன் வளர்சிதை மாற்றமடையாமல் இருக்கிறது என சில உயிர்வேதியியல் பாடப்புத்தகங்கள் மற்றும் நடப்பு ஆராய்ச்சி வெளியீடுகள் தெரிவிக்கின்றன [19]. இக்கோட்பாட்டுக்கு எதிரான ஆதாரங்களும் கிடைக்கின்றன. 30 ஆண்டுகளுக்கு முன்னால் உட்செலுத்தப்பட்ட ஐசோபுரோபனாலை ஆக்சிசனேற்றமடையச் செய்து அசிட்டோன் உருவாக்க முடியுமெனக் கூறப்படுகிறது. அல்லது உடலிலுள்ள அசிட்டோ அசிட்டிக் பொருள்கள் நொதிகளால் தன்னிச்சையாக உடைந்தும் அசிட்டோன் உருவாக முடியும் என்றும் கூறப்படுகிறது.
மேற்கோள்கள்
தொகு- ↑ Merck Index, 11th Edition, 58
- ↑ 2.0 2.1 2.2 "Acetone". NIST Chemistry WebBook. USA: National Institute of Standards and Technology.
- ↑ Klamt, Andreas (2005). COSMO-RS: From Quantum Chemistry to Fluid Phase Thermodynamics and Drug Design. Elsevier. pp. 92–94. பன்னாட்டுத் தரப்புத்தக எண் 0444519947.
- ↑ Ash, Michael; Ash, Irene (2004). Handbook of preservatives. Synapse Information Resources, Inc. p. 369. பன்னாட்டுத் தரப்புத்தக எண் 1890595667.
- ↑ "Acetone – PubChem Public Chemical Database". The PubChem Project. USA: National Center for Biotechnology Information.
- ↑ "Acetone CHROMASOLV® Plus, for HPLC, ≥99.9%". Sigma-Aldrich. பார்க்கப்பட்ட நாள் 15 September 2011.
- ↑ Acetone, World Petrochemicals report, January 2010
- ↑ Stylianos Sifniades, Alan B. Levy, "Acetone" in Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim, 2005.
- ↑ Gorman, Mel; Doering, Charles (1959). "History of the structure of acetone". Chymia 5: 202–208.
- ↑ Dumas, J. (1832) "Sur l'esprit pyro-acétique" (On pyro-acetic spirit), Annales de Chimie et de Physique, 2nd series, 49 : 208–210.
- ↑ Liebig, Justus (1832) "Sur les combinaisons produites par l'action du gas oléfiant et l'esprit acétique" (On compounds produced by the action of ethylene and acetic spirit), Annales de Chimie et de Physique, 2nd series, 49 : 146–204 (especially 193–204).
- ↑ Bussy, Antoine (1833) "De quelques Produits nouveaux obtenus par l’action des Alcalis sur les Corps gras à une haute température" (On some new products obtained by the action of alkalies on fatty substances at a high temperature), Annales de Chimie et de Physique, 2nd series, 53 : 398–412 ; see footnote on pp. 408–409.
- ↑ Williamson, A. W. (1852) "On Etherification," Journal of the Chemical Society, 4 : 229–239 ; (especially pp. 237–239).
- ↑ Gerhardt, Charles (1853) "Researches sur les acids organiques anhydres" (Research on anhydrous organic acids), Annales de Chimie et de Physique, 3rd series, 37 : 285–342 ; see p. 339.
- ↑ Kekulé, Auguste (1865) "Sur la constitution des substances aromatiques," Bulletin de la Société chimique de Paris, 1 : 98–110 ; (especially p. 110).
- ↑ Kekulé, Auguste (1866) "Untersuchungen über aromatischen Verbindungen" (Investigations into aromatic compounds), Annalen der Chemie und Pharmacie, 137 : 129–196 ; (especially pp. 143–144).
- ↑ Loschmidt, J. (1861) Chemische Studien Vienna, Austria-Hungary: Carl Gerold's Sohn.
- ↑ Chaim Weizmann. chemistryexplained.com
- ↑ Vujasinovic, M; Kocar, M; Kramer, K; Bunc, M; Brvar, M (2007). "Poisoning with 1-propanol and 2-propanol". Human & Experimental Toxicology 26 (12): 975. doi:10.1177/0960327107087794.