இசுட்ரோன்சியம் புளோரைடு
இசுட்ரோன்சியம் புளோரைடு (Strontium fluoride) என்பது SrF2 என்ற மூலக்கூற்று வாய்ப்பாட்டால் விவரிக்கப்படும் ஒரு கனிம வேதியியல் சேர்மம் ஆகும். இசுட்ரோன்சியம்(II) புளோரைடு , இசுட்ரோன்சியம் இருபுளோரைடு, இசுட்ரோன்சியம் டைபுளோரைடு என்ற பெயர்களாலும் இச்சேர்மம் அறியப்படுகிறது. இசுட்ரோன்சியத்தின் புளோரைடு உப்பான இது நொறுங்கக் கூடியதாகவும் வெண்மையான படிகத் திண்மமாகவும் காணப்படுகிறது. இயற்கையில் இசுட்ரோன்சியோபுளோரைட்டு கனிமம் போன்ற தோற்றத்தில் இக்கனிமம் காணப்படுகிறது.[2][3]
| |
| பெயர்கள் | |
|---|---|
| வேறு பெயர்கள்
இசுட்ரோன்சியம் டைபுளோரைடு
இசுட்ரோன்சியம்(II) புளோரைடு | |
| இனங்காட்டிகள் | |
| 7783-48-4 | |
| ChemSpider | 74190 |
| EC number | 232-00-3 |
| யேமல் -3D படிமங்கள் | Image |
| பப்கெம் | 82210 |
| |
| UNII | EFY8GJS81Z |
| பண்புகள் | |
| SrF2 | |
| வாய்ப்பாட்டு எடை | 125.62 கி/மோல் |
| அடர்த்தி | 4.24 கி/செ.மீ3 |
| உருகுநிலை | 1,473 °C (2,683 °F; 1,746 K) |
| கொதிநிலை | 2,460 °C (4,460 °F; 2,730 K) |
| 0.117 கி/100 மில்லி லிட்டர் | |
கரைதிறன் பெருக்கம் (Ksp)
|
4.33×10−9[1] |
| −37.2·10−6 செ.மீ3/மோல் | |
| ஒளிவிலகல் சுட்டெண் (nD) | 1.439 @0.58 μm |
| கட்டமைப்பு | |
| படிக அமைப்பு | கனசதுரம் (படிக முறை), cF12 |
| புறவெளித் தொகுதி | Fm3m, #225 |
| Lattice constant | a = 5.80 Å, b = 5.80 Å, c = 5.80 Å |
படிகக்கூடு மாறிலி
|
|
| Sr, 8, கனசதுரம் F, 4, நான்முகி | |
| தீங்குகள் | |
| தீப்பற்றும் வெப்பநிலை | எளிதில் தீப்பற்றாது |
| தொடர்புடைய சேர்மங்கள் | |
| ஏனைய எதிர் மின்னயனிகள் | இசுட்ரோன்சியம் குளோரைடு இசுட்ரோன்சியம் புரோமைடு இசுட்ரோன்சியம் அயோடைடு |
| ஏனைய நேர் மின்அயனிகள் | பெரிலியம் புளோரைடு மக்னீசியம் புளோரைடு கால்சியம் புளோரைடு பேரியம் புளோரைடு |
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |
தயாரிப்பு
தொகுஐதரோபுளோரிக் அமிலத்துடன் இசுட்ரோன்சியம் கார்பனேட்டைச் சேர்த்து வினைபுரியச் செய்து இசுட்ரோன்சியம் புளோரைடு தயாரிக்கப்படுகிறது.[4]
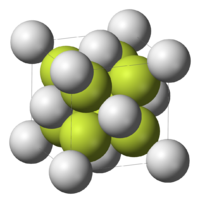
கட்டமைப்பு
தொகுஇசுட்ரோன்சியம் புளோரைடு புளோரைட்டு கட்டமைப்பை ஏற்றுக்கொள்கிறது. வாயு நிலையில் SrF2 என்ற இம்மூலக்கூறு நேரியல் அல்லாத அமைப்புடன் F−Sr−F கோணம் தோராயமாக 120° அளவைக் கொண்டுள்ளது.[5] இணைதிறன் கூடு இலத்திரன் சோடிகளின் தள்ளுகைக் கொள்கைக்கு கோட்பாட்டிற்கு இது விதிவிலக்காகும். ஏனெனில் இக்கொள்கை ஒரு நேரியல் கட்டமைப்பைக் கணிக்கும். இணைதிறன் கூட்டுக்கு கீழே உள்ள கூட்டில் உள்ள d ஆர்பிட்டால்களின் பங்களிப்புகள் பொறுப்பு என்று முன்மொழிவதற்கு தொடக்க நிலை கணக்கீடுகள் மேற்கோள் காட்டப்பட்டுள்ளன.[6] மற்றொரு முன்மொழிவு என்னவென்றால், இசுட்ரோன்சியம் அணுவின் எலக்ட்ரான் மையத்தின் முனைப்புத்திறன் Sr−F பிணைப்புகளுடன் தொடர்பு கொள்ளும் தோராயமான மின்னழுத்த விநியோகத்தை உருவாக்குகிறது.[7]
பண்புகள்
தொகுஇசுட்ரோன்சியம் புளோரைடு கிட்டத்தட்ட நீரில் கரையாது. 25 பாகை செல்சியசு வெப்பநிலையில் இதன் கரைதிறன் சமநிலை அளவு (Ksp) தோராயமாக 2.0x10−10 ஆகும்.
கண்கள் மற்றும் தோலில் இசுட்ரோன்சியம் புளோரைடு எரிச்சலூட்டும். உள்ளிழுக்கும் போது அல்லது உட்கொள்ளும்போது தீங்கு விளைவிக்கும். CaF2 மற்றும் BaF2 சேர்மங்கள் போன்றே, SrF2 உயர்ந்த வெப்பநிலையில் மீ அயன கடத்துத்திறனைக் காட்டுகிறது.[8]
இசுட்ரோன்சியம் புளோரைடு வெற்றிட புற ஊதா (150 nm) முதல் அகச்சிவப்பு (11 μm) வரையிலான அலைநீளங்களில் ஒளி புகும் தன்மை கொண்டதாக உள்ளது. இதன் ஒளியியல் பண்புகள் கால்சியம் புளோரைடு மற்றும் பேரியம் புளோரைடு ஆகியற்றுக்கு இடைநிலையில் உள்ளன.[9]
பயன்கள்
தொகுஇசுட்ரோன்சியம் புளோரைடு ஒரு சிறிய அளவிலான சிறப்புப் பயன்பாடுகளுக்கு ஒளியியல் பொருளாகப் பயன்படுத்தப்படுகிறது. எடுத்துக்காட்டாக, வில்லைகள் மீது ஒளியியல் பூச்சு போன்ற பயன்பாடுகளில் இது பயன்படுத்தப்படுகிறது.
கதிரியக்க ஐசோடோப் வெப்பமின் உற்பத்தி இயந்திரங்களில் கதிரியக்க ஐசோடோப்பு கடத்தியாக இசுட்ரோன்சியம் -90 பயன்படுத்தப்படுகிறது.
மேற்கோள்கள்
தொகு- ↑ John Rumble (June 18, 2018). CRC Handbook of Chemistry and Physics (in English) (99 ed.). CRC Press. pp. 5–189. பன்னாட்டுத் தரப்புத்தக எண் 978-1138561632.
{{cite book}}: CS1 maint: unrecognized language (link) - ↑ "Strontiofluorite".
- ↑ "List of Minerals". 21 March 2011.
- ↑ W. Kwasnik (1963). "Strontium Fluoride". In G. Brauer (ed.). Handbook of Preparative Inorganic Chemistry, 2nd Ed. Vol. 1. NY, NY: Academic Press. p. 234.
- ↑ Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ed.). Butterworth-Heinemann. பன்னாட்டுத் தரப்புத்தக எண் 0080379419.
- ↑ Ab initio model potential study of the equilibrium geometry of alkaline earth dihalides: MX2 (M = Mg, Ca, Sr, Ba; X=F, Cl, Br, I)Seijo L.,Barandiarán Z J. Chem. Phys. 94, 3762 (1991) எஆசு:10.1063/1.459748
- ↑ Core Distortions and Geometries of the Difluorides and Dihydrides of Ca, Sr, and Ba Bytheway I, Gillespie RJ, Tang TH, Bader RF Inorganic Chemistry, Vol.34, No.9, 2407-2414, 1995 எஆசு:10.1021/ic00113a023
- ↑ "Newmet Koch - Strontium". Archived from the original on 2005-12-14.
- ↑ Mediatopia Ltd. "Strontium Fluoride (SrF2) Optical Material". Crystran.co.uk. பார்க்கப்பட்ட நாள் 2012-08-18.