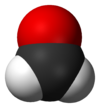
பார்மால்டிகைடு
பார்மால்டிகைடு (Formaldehyde) என்பது CH2O (H−CHO) என்ற மூலக்கூற்று வாய்ப்பாட்டால் விவரிக்கப்படும் ஒரு கரிம வேதியியல் சேர்மமாகும். இயற்கையில் கிடைக்கும் இக்கரிமச் சேர்மம் ஓர் எளிய ஆல்டிகைடுக்கு எடுத்துக்காட்டு ஆகும். பார்மிக்காடியுடன் நெருங்கிய தொடர்பு கொண்டிருப்பதால் பார்மால்டிகைடு என்ற பொதுப்பெயர் வழங்கப்படுகிறது.
| |||

| |||
| பெயர்கள் | |||
|---|---|---|---|
| விருப்பத்தெரிவு ஐயூபிஏசி பெயர்
பார்மால்டிகைடு[1] | |||
| முறையான ஐயூபிஏசி பெயர்
மெத்தனல்[1] | |||
| வேறு பெயர்கள்
மெத்தில் ஆல்டிகைடு
மெத்திலீன் கிளைக்கால் (நீரிய கரைசலில் டையால் உருவாகிறது) மெத்திலீன் ஆக்சைடு பார்மலின் (நீரிய கரைசல்) பார்மால் கார்பனைல் ஐதரைடு | |||
| இனங்காட்டிகள் | |||
| 50-00-0 | |||
| 3DMet | B00018 | ||
Beilstein Reference
|
1209228 | ||
| ChEBI | CHEBI:16842 | ||
| ChEMBL | ChEMBL1255 | ||
| ChemSpider | 692 | ||
| DrugBank | DB03843 | ||
| EC number | 200-001-8 | ||
Gmelin Reference
|
445 | ||
IUPHAR/BPS
|
4196 | ||
| யேமல் -3D படிமங்கள் | Image | ||
| KEGG | D00017 | ||
| ம.பா.த | பார்மால்டிகைடு | ||
| பப்கெம் | 712 | ||
| வே.ந.வி.ப எண் | LP8925000 | ||
| |||
| UNII | 1HG84L3525 | ||
| UN number | 2209 | ||
| பண்புகள் | |||
| CH2O | |||
| வாய்ப்பாட்டு எடை | 30.03 g·mol−1 | ||
| தோற்றம் | நிறமற்ற வாயு | ||
| அடர்த்தி | 0.8153 கி/செ.மீ3 (−20 °செல்சியசு)[2] | ||
| உருகுநிலை | −92 °C (−134 °F; 181 K) | ||
| கொதிநிலை | −19 °C (−2 °F; 254 K)[2] | ||
| 400 கி/லிட்டர் | |||
| மட. P | 0.350 | ||
| ஆவியமுக்கம் | < 1 வளிமண்டல அழுத்தம்[3] | ||
| காடித்தன்மை எண் (pKa) | 13.27 (நீரேற்று) [4][5] | ||
| −18.6·10−6 செ.மீ3/மோல் | |||
| இருமுனைத் திருப்புமை (Dipole moment) | 2.330 D[6] | ||
| கட்டமைப்பு | |||
| மூலக்கூறு வடிவம் | |||
| தீங்குகள் | |||
| பொருள் பாதுகாப்பு குறிப்பு தாள் | MSDS(Archived) | ||
| GHS pictograms |    
| ||
| GHS signal word | அபாயம் | ||
| H301, H311, H331, H314, H317, H335, H336, H341, H350, H370 | |||
| P201, P280, P303+361+353, P304+340, P309+311, P305+351+338 | |||
| தீப்பற்றும் வெப்பநிலை | 64 °C (147 °F; 337 K) | ||
Autoignition
temperature |
430 °C (806 °F; 703 K) | ||
| வெடிபொருள் வரம்புகள் | 7–73% | ||
| Lethal dose or concentration (LD, LC): | |||
LD50 (Median dose)
|
100 மி.கி/கி.கி (வாய்வழி, எலி)[9] | ||
LC50 (Median concentration)
|
மில்லியனுக்கு 333 பகுதிகள் (சுண்டெலி, 2 h) மில்லியனுக்கு 815 பகுதிகள் (எலி, 30 நிமிடம்)[10] | ||
LCLo (Lowest published)
|
மில்லியனுக்கு 333 பகுதிகள் (எலி, 2 h)[10] | ||
| அமெரிக்க சுகாதார ஏற்பு வரம்புகள்: | |||
அனுமதிக்கத்தக்க வரம்பு
|
TWA மில்லியனுக்கு 0.75 பகுதிகள் ST மில்லியனுக்கு 2 பகுதிகள் (பார்மால்டிகைடாகவும் பார்மலினாகவும்)[7][8] | ||
பரிந்துரைக்கப்பட்ட வரம்பு
|
Ca TWA மில்லியனுக்கு 0.016 பகுதிகள் C மில்லியனுக்கு 0.1 பகுதிகள் [15-நிமிடம்][7] | ||
உடனடி அபாயம்
|
Ca [மில்லியனுக்கு 20 பகுதிகள்][7] | ||
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |||
பல்வேறு வேதிச் சேர்மங்களின் தயாரிப்புக்கு பார்மால்டிகைடு ஒரு முன்னோடிச் சேர்மமாக உள்ளது. 1996 ஆம் ஆண்டு நிலவரப்படி ஆண்டுக்கு 8.7 மில்லியன் டன் பார்மால்டிகைடு உற்பத்தி செய்யப்பட்டது [11]. குறைந்த அடர்த்தி மரப்பலகை மற்றும் வண்ணப்பூச்சுகளுக்கான தொழிற்சாலை பிசின்கள் தயரிப்பில் பார்மால்டிகைடு முக்கியமாகப் பயன்படுகிறது.
பரவலாகப் பயன்பாட்டில் உள்ளதால் இதன் நச்சுத்தன்மையும் எளிதில் ஆவியாகும் தன்மையும் மனித உடல் நலத்திற்கு குறிப்பிடத்தக்க அபாயத்தை ஏற்படுத்துவதாகக் கருதப்படுகிறது [12][13]. பார்மால்டிகைடு சேர்மத்தால் மனிதர்களுக்கு புற்றுநோய் ஏற்படும் அபாயம் உள்ளது என அமெரிக்காவின் தேசிய நச்சுயியல் அமைப்பு 2011 ஆம் ஆண்டு அறிவித்துள்ளது [14][15][16].
வரலாறு
தொகுமுதன் முதலாக இரசிய வேதியியலாளா் அலெக்சாண்டா் புட்லெரோவ் (1828–86) என்பவரால் பார்மால்டிகைடு என்ற சேர்மத்தின் இருப்பு அறிவிக்கப்பட்டது. (1828–86) ஆனால், இவா் பார்மால்டிகைடை டை-ஆக்சிமெதிலீன் என அழைத்தாா்.[17] இறுதியாக ஆகஸ்ட் வில்லெம் வான் ஆபுமன் என்பவரால் பார்மால்டிகைடின் சரியான வடிவம் மற்றும் தயாாிப்பு 1869 ஆம் ஆண்டு கண்டுபிடிக்கப்பட்டது.[18][19]
பார்மால்டிகைடின் வடிவங்கள்
தொகுபல எளிய கார்பன் சோ்மங்களோடு ஒப்பிடும் போது பார்மால்டிகைடு சற்றே சிக்கலான வெவ்வேறு வடிவங்களைப் பெற்றுள்ளது. ஒரு வளிமமாக பார்மால்டிகைடு நிறமற்ற வளிமமாகும். காரமான எரிச்சலூட்டும் மணம் இச்சேர்மத்தை அடையாளப்படுத்துகிறது. ஒடுக்கும் வினைக்கு உட்படுத்தும்போது இவ்வாயு பார்மால்டிகைடின் வெவ்வேறு மூலக்கூற்று வாய்ப்பாடு கொண்ட பிற வடிவங்களாக மாறுகிறது. இவையனைத்தும் பல்வேறு நடைமுறை பயன்களைக் கொண்டுள்ளன. 1,3,5-டிரையாக்சேன் எனப்படும் வளைய முப்படி மெட்டா பார்மால்டிகைடு ஒரு முக்கியமான பார்மால்டிகைடு வழிப்பெறுதியாகும். இதன் மூலக்கூற்று வாய்ப்பாடு (CH2O)3 ஆகும். பாராபார்மால்டிகைடு என்ற நேரியல் பலபடியும் நன்கு அறியப்படுகிறது. இச்சேர்மங்கள் யாவும் ஒத்த வேதியியல் பண்புகளையும் பெரும்பாலும் ஒன்றுக்கு மாற்றாக மற்றொரு சேர்மத்தைப் பயன்படுத்திக் கொள்ளும் வகையிலும் உள்ளன.
பார்மால்டிகைடை நீரில் கரைக்கும் போது மெத்தேன்டையால் என்ற நீரேற்றாக உருவாகிறது. இதன் மூலக்கூற்று வாய்ப்பாடு H2C(OH)2 ஆகும். இக்கரைசலின் செறிவு மற்றும் வெப்பநிலைக்கு ஏற்ப இச்சேர்மம் பல்வேறு வகையான சில்படிமங்களாக காணப்படுகிறது. 40 சதவீத பார்மால்டிகைடை கொண்ட பூரித நீர்க்கரைசல் அல்லது நிறையளவில் 37 சதவீத அளவு கொண்ட பார்மால்டிகைடு கரைசல் 100 சதவீத பார்மலின் என்று அழைக்கப்படுகிறது. மெத்தனால் போன்ற நிலைப்படுத்தி கரைசலுடன் சிறிதளவு சேர்க்கப்பட்டு ஆக்சிசனேற்ற வினையும் பலபடியாதல் வினையும் அடக்கப்படுகிறது. வணிகரீதியிலான பார்மலின் 10–12% மெதனாலைக் கொண்டிருக்கிறது. பார்மலின் என்ற வணிகப் பெயரானது வணிகரீதியில் மிக நீண்ட நெடுங்காலமாகப் பயன்படுத்தப்பட்டு வருகிறது[20]
தோற்றம்
தொகுசுற்றுச்சூழலிலுள்ள மொத்த பார்மால்டிகைடு அளவில் 90% வரை மேல் வளிமண்டலத்திலுள்ள செயல்முறைகள் மூலம் பங்களிக்கப்படுகின்றன. காட்டுத்தீ, வாகனப் புகை, புகையிலை புகை போன்ற கார்பன் சேர்மங்கள் மற்றும் மீத்தேனின் ஆக்சிசனேற்றம் அல்லது மீத்தேன் எரிப்பு வினையில் பார்மால்டிகைடு ஓர் இடைநிலை விளைபொருளாகும். வளிமண்டலத்திலுள்ள மீத்தேன் மற்றும் பிற ஐதரோகார்பன்கள் மீது சூரிய ஒளி, ஆக்சிசன் ஆகியவற்றின் வினையால் பார்மால்டிகைடு வளிமண்டலத்தில் உற்பத்தி செய்யப்படுகிறது.
பனிப்புகையின் ஒரு பகுதியாக பார்மால்டிகைடு உருவாகிறது.
விண்வெளிக்கு அப்பாலுள்ள புறவெளியிலும் பார்மால்டிகைடு கண்டறியப்பட்டுள்ளது.
பார்மால்டிகைடும் அதன் கூட்டுசேர்க்கை பொருள்களும் உயிரினங்களில் எங்கும் காணப்படுகின்றன. மனிதர்கள் மற்றும் பிற விலங்குகளின் இரத்த ஓட்டத்தில் சுமார் 0.1 மில்லிமோலார் செறிவு பார்மால்டிகைடு காணப்படுகிறது [21].
தொழில்முறை தயாாிப்பு
தொகுபாா்மால்டிகைடானது தொழில் முறையில் மெத்தனால் -இனை வினைவேக மாற்றி முன்னிலையில் ஆக்சிசனேற்றம் செய்வதன் மூலம் தயாாிக்கப்படுகிறது. இந்த வினையில், வெள்ளி உலோகம் அல்லது இரும்பு ஆக்சைடு மற்றும் மாலிப்டினம் ஆக்சைடு கலந்த கலவை அல்லலது வெனடியம் பெண்டாக்சைடு ஆகியவை பொதுவாகப் பயன்படுத்தப்படும் வினைவேக மாற்றிகளாகும். பொதுவாகப் பயன்படுத்தப்படும் பார்மாக்சு வினையில் மெத்தனால் மற்றும் ஆக்சிசன் ஆகியவை ca. 250–400 °C வெப்பநிலையில் மாலிப்டினம் மற்றும் வெனடியம் உடன் இரும்பு ஆக்சைடு அல்லது வெனடியம் உடன் இரும்பு ஆக்சைடு முன்னிலையில் பின்வரும் வேதிச்சமன்பாட்டின்படி வினைபுாிந்து பார்மால்டிகைடைத் தருகின்றன. :[11]
- 2 CH3OH + O2 → 2 CH2O + 2 H2O
வெள்ளியை அடிப்படையாகக் கொண்ட வினைவேகமாற்றி முன்னிலையில் பொதுவாக உயா் வெப்பநிலையில் (அதாவது 650 °C) மேலே குறிப்பிடப்பட்ட வேதிவினையும், ஹைட்ரஜன் நீக்க வினையும் ஒரே நேரத்தில் நடைபெற்று பார்மால்டிகைடைத் தருகிறது.
- CH3OH → CH2O + H2
கொள்கை அளவில் பார்மால்டிகைடை மீத்தேனை ஆக்சிசனேற்றம் செய்தும் பெற முடியும். ஆனால், தொழில் முறையில் மீத்தேனை ஆக்சிசனேற்றம் செய்வதை விட மெத்தனாலை ஆக்சிசனேற்றம் செய்வது எளிதானதாக இருக்கிறது.
தொழிற்துறை பயன்கள்
தொகுபார்மால்டிகைடானது பல சிக்கலான சோ்மங்கள் மற்றும் பொருட்களின் பொதுவான முன்னோடி சோ்மமாக உள்ளது. யூாியா பார்மால்டிகைடு பிசின், மேலமைன் பிசின், பீனால் பார்மால்டிகைடு பிசின், பாலிஆக்சிமெதிலீன் நெகிழிகள், 1,4-பியூட்டேன்டையால் ஆகியவை பார்மால்டிடைட்டிலிருந்து பெறப்படும் சிக்கலான பொருட்களாகும்.[11] ஜவுளித்துறையில் பார்மால்டிஹைடை அடிப்படையாகக் கொண்ட பிசின்களை துணிகளை இறுதி செய்யும் பணியில் துணிகளில் கறை படியாமல் இருக்கச் செய்வதற்காக பயன்படுத்துகின்றனா்.[22] பார்மால்டிகைடை அடிப்படையாகக் கொண்ட பொருட்கள் தானியங்கி வாகனங்களின் உற்பத்திக்கு முக்கியமான ஒலிபரப்பு, மின் அமைப்பு, இயந்திர தொகுதி, கதவு பேனல்கள், அச்சுகள் மற்றும் நிறுத்த மிதி ஆகியவற்றிற்கான கூறுகளை உருவாக்க பயன்படுத்தப்படுகின்றன. 2003 ஆம் ஆண்டில் பார்மால்டிஹைடு மற்றும் அதன் வழிப்பொருட்களின் தயாரிப்புகளின் விற்பனை மதிப்பு 145 பில்லியன் டாலருக்கும் அதிகமாக இருந்தது, அமெரிக்கா மற்றும் கனடா மொத்த உள்நாட்டு உற்பத்தியில் 1.2% ஆக இருந்தது. மறைமுக வேலைவாய்ப்பு உட்பட, அமெரிக்க மற்றும் கனடாவில் 11,900 ஆலைகளில், சுமார் 4 மில்லியன் மக்களுக்கு பார்மால்டிகைடு தொழிலில் வேலைவாய்ப்பு கிடைத்தது.[23]
பார்மால்டிகைடை பீனால், யூரியா, மேலமீன், ஆகியவற்றுடன் வினைப்படுத்தும் போது முறையே, வெப்பத்தால் இறுகும் பீனால் பார்மால்டிகைடு பிசின், யூாியா பார்மால்டிஹைடு பிசின், மேலமீன் பிசின் ஆகியவை உருவாக்கப்படுகின்றன. இந்தப் பலபடி மூலக்கூறுகள் ஒட்டுபலகைகள் மற்றும் கம்பளவிாிப்புகளுக்கான பொதுவான மற்றும் நிரந்தரமான ஒட்டும் பசைகளாகின்றன.
மேற்கோள்கள்
தொகு- ↑ 1.0 1.1 "Front Matter". Nomenclature of Organic Chemistry : IUPAC Recommendations and Preferred Names 2013 (Blue Book). Cambridge: The Royal Society of Chemistry. 2014. p. 908. எண்ணிம ஆவணச் சுட்டி:10.1039/9781849733069-FP001. பன்னாட்டுத் தரப்புத்தக எண் 978-0-85404-182-4.
- ↑ 2.0 2.1 "SIDS Initial Assessment Report" (PDF). International Programme on Chemical Safety. Archived from the original (PDF) on 2019-03-28. பார்க்கப்பட்ட நாள் 2019-04-21.
- ↑ Spence, Robert; Wild, William (1935). "114. The vapour-pressure curve of formaldehyde, and some related data". Journal of the Chemical Society (Resumed): 506–509. doi:10.1039/jr9350000506.
- ↑ "PubChem Compound Database; CID=712". National Center for Biotechnology Information. Archived from the original on 2019-04-12. பார்க்கப்பட்ட நாள் 2017-07-08.
- ↑ "Acidity of aldehydes". Chemistry Stack Exchange. Archived from the original on 2018-09-01. பார்க்கப்பட்ட நாள் 2019-04-21.
- ↑ Nelson Jr., R. D.; Lide, D. R.; Maryott, A. A. (1967). "Selected Values of electric dipole moments for molecules in the gas phase (NSRDS-NBS10)" (PDF). Archived (PDF) from the original on 2018-06-08. பார்க்கப்பட்ட நாள் 2019-04-21.
- ↑ 7.0 7.1 7.2 "NIOSH Pocket Guide to Chemical Hazards #0293". National Institute for Occupational Safety and Health (NIOSH).
- ↑ "NIOSH Pocket Guide to Chemical Hazards #0294". National Institute for Occupational Safety and Health (NIOSH).
- ↑ "Substance Name: Formaldehyde [USP]". ChemlDplus. US National Library of Medicine. Archived from the original on 2017-09-18.
- ↑ 10.0 10.1 "Formaldehyde". Immediately Dangerous to Life and Health. National Institute for Occupational Safety and Health (NIOSH).
- ↑ 11.0 11.1 11.2 Günther Reuss, Walter Disteldorf, Armin Otto Gamer, Albrecht Hilt "Formaldehyde" in Ullmann's Encyclopedia of Industrial Chemistry, 2002, Wiley-VCH, Weinheim. எஆசு:10.1002/14356007.a11_619.
- ↑ "Formaldehyde", Formaldehyde, 2-Butoxyethanol and 1-tert-Butoxypropan-2-ol (PDF), IARC Monographs on the Evaluation of Carcinogenic Risks to Humans 88, Lyon, France: International Agency for Research on Cancer, 2006, pp. 39–325, பன்னாட்டுத் தரப்புத்தக எண் 978-92-832-1288-1
- ↑ "Formaldehyde (gas)", Report on Carcinogens, Eleventh Edition (PDF), U.S. Department of Health and Human Services, Public Health Service, National Toxicology Program, 2005
- ↑ Harris, Gardiner (2011-06-10). "Government Says 2 Common Materials Pose Risk of Cancer". த நியூயார்க் டைம்ஸ் இம் மூலத்தில் இருந்து 2019-03-28 அன்று. பரணிடப்பட்டது.. https://web.archive.org/web/20190328042744/https://www.nytimes.com/2011/06/11/health/11cancer.html. பார்த்த நாள்: 2011-06-11.
- ↑ National Toxicology Program (2011-06-10). "12th Report on Carcinogens". National Toxicology Program. Archived from the original on 2011-06-08. பார்க்கப்பட்ட நாள் 2011-06-11.
- ↑ National Toxicology Program (2011-06-10). "Report On Carcinogens - Twelfth Edition - 2011" (PDF). National Toxicology Program. Archived from the original on 2011-06-12. பார்க்கப்பட்ட நாள் 2011-06-11.
- ↑ A. Butlerow (1859) "Ueber einige Derivate des Jodmethylens" (On some derivatives of methylene iodide), Annalen der Chemie und Pharmacie, vol . 111, pages 242–252. In this paper, Butlerov discovered formaldehyde, which he called "Dioxymethylen" (methylene dioxide) [page 247] because his empirical formula for it was incorrect (C4H4O4).
- ↑ In 1867, A. W. Hofmann first announced to the Royal Prussian Academy of Sciences the production of formaldehyde by passing methanol vapor in air over hot platinum wire. See: A. W. Hofmann (14 October 1867) "Zur Kenntnis des Methylaldehyds" ([Contributions] to our knowledge of methylaldehyde), Monatsbericht der Königlich Preussischen Akademie der Wissenschaften zu Berlin (Monthly Report of the Royal Prussian Academy of Sciences in Berlin), vol. 8, pages 665–669. Reprinted in:
- A.W. Hofmann, (1868) "Zur Kenntnis des Methylaldehyds", Annalen der Chemie und Pharmacie (Annals of Chemistry and Pharmacy), vol. 145, no. 3, pages 357–361.
- A.W. Hofmann (1868) "Zur Kenntnis des Methylaldehyds", Journal für praktische Chemie (Journal for Practical Chemistry), vol. 103, no. 1, pages 246–250.
- Hofmann, A.W. (1869). "Beiträge zur Kenntnis des Methylaldehyds". Journal für Praktische Chemie 107 (1): 414–424. doi:10.1002/prac.18691070161. https://books.google.com/books?id=2AIwAAAAIAAJ&pg=PA414#v=onepage&q&f=false.
- A.W. Hofmann (1869) "Beiträge zur Kenntnis des Methylaldehyds," Berichte der Deutschen Chemischen Gesellschaft (Reports of the German Chemical Society), vol. 2, pages 152–159.
- ↑ Read, J. (1935). Text-Book of Organic Chemistry. London: G Bell & Sons.
- ↑ Merriam-Webster, Merriam-Webster's Collegiate Dictionary, Merriam-Webster, archived from the original on 2020-10-10, பார்க்கப்பட்ட நாள் 2017-05-09.
- ↑ National Research Council (2014). Review of the Formaldehyde Assessment in the National Toxicology Program 12th Report on Carcinogens (PDF). Washington, DC: The National Academies Press. p. 91. எண்ணிம ஆவணச் சுட்டி:10.17226/18948. பன்னாட்டுத் தரப்புத்தக எண் 978-0-309-31227-1. PMID 25340250.
{{cite book}}: Invalid|ref=harv(help) - ↑ "Formaldehyde in Clothing and Textiles FactSheet". NICNAS. Australian National Industrial Chemicals Notification and Assessment Scheme. May 2013. Archived from the original on 13 நவம்பர் 2014. பார்க்கப்பட்ட நாள் 12 November 2014.
- ↑ Economic Importance, Formaldehyde Council. 2009. Accessed on April 14, 2010.
புற இணைப்புகள்
தொகு- International Chemical Safety Card 0275 (gas)
- International Chemical Safety Card 0695 (solution)
- Formaldehyde from ChemSub Online
- Prevention guide—Formaldehyde in the Workplace (PDF) from the IRSST
- Formaldehyde from the National Institute for Occupational Safety and Health
- SIDS Initial Assessment Report for Formaldehyde பொருளியல் கூட்டுறவு மற்றும் வளர்ச்சிக்கான அமைப்பு (OECD) இல் இருந்து
- Formaldehyde Added to "Known Carcinogens" List Despite Lobbying by Chemical Industry — video report by Democracy Now!
- Do you own a post-Katrina FEMA trailer? Check your VIN#
- So you’re living in one of FEMA’s Katrina trailers... What can you do?