பொட்டாசியம் கார்பனேட்டு
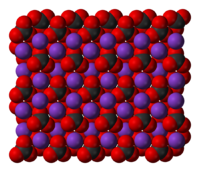
பொட்டாசியம் கார்பனேட் என்ற வேதிச்சேர்மத்தின் மூலக்கூறு வாய்ப்பாடு (K2CO3) ஆகும். இது ஒரு வெள்ளை நிற உப்பு ஆகும். நீரில் கரையகிறது. எத்தனாலில் கரைவதில்லை. இது வலிமையான காரக்கரைசலை உருவாக்குகிறது. கார்பனீராக்சைடு உடன் பாெட்டாசியம் ஐதராக்சைடு உறிஞ்சு வினையின் மூலமாக இது தயாரிக்கப்படுகிறது. இது ஒரு நீர்உறிஞ்சும் பொருளாகும். பெரும்பாலும் ஈரமான திண்மமாக காணப்படுகிறது. பொட்டாசியம் கார்பனேட், சோப்பு மற்றும் கண்ணாடி உற்பத்தி செய்யப் பயன்படுத்தப்படுகிறது.
| |
| |

| |
| பெயர்கள் | |
|---|---|
| ஐயூபிஏசி பெயர்
Potassium carbonate
| |
| வேறு பெயர்கள்
Carbonate of potash, Dipotassium carbonate, Sub-carbonate of potash, Pearl ash, Potash, Salt of tartar, Salt of wormwood.
| |
| இனங்காட்டிகள் | |
| 584-08-7 | |
| ChEBI | CHEBI:131526 |
| ChemSpider | 10949 |
| யேமல் -3D படிமங்கள் | Image |
| பப்கெம் | 11430 |
| வே.ந.வி.ப எண் | TS7750000 |
| |
| UNII | BQN1B9B9HA |
| பண்புகள் | |
| K2CO3 | |
| வாய்ப்பாட்டு எடை | 138.205 g/mol |
| தோற்றம் | white, நீர் உறிஞ்சும் திறன் solid |
| அடர்த்தி | 2.43 g/cm3 |
| உருகுநிலை | 891 °C (1,636 °F; 1,164 K) |
| கொதிநிலை | decomposes |
| 112 g/100 mL (20 °C) 156 g/100 mL (100 °C) | |
| கரைதிறன் | 3.11 g/100 mL (25 °C) மெத்தனால் insoluble in மதுசாரம், அசிட்டோன் |
| −59.0·10−6 cm3/mol | |
| தீங்குகள் | |
| பொருள் பாதுகாப்பு குறிப்பு தாள் | ICSC 1588 |
| GHS pictograms | 
|
| GHS signal word | Warning |
| H302, H315, H319, H335 | |
| P261, P305+351+338 | |
| தீப்பற்றும் வெப்பநிலை | Non-flammable |
| Lethal dose or concentration (LD, LC): | |
LD50 (Median dose)
|
1870 mg/kg (oral, rat)[1] |
| தொடர்புடைய சேர்மங்கள் | |
| ஏனைய எதிர் மின்னயனிகள் | பொட்டாசியம் பைகார்பனேட்டு |
| ஏனைய நேர் மின்அயனிகள் | Lithium carbonate சோடியம் கார்பனேட்டு ருபீடியம் கார்பனேட்டு Caesium carbonate |
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |
வரலாறு
தொகுபொட்டாசியம் கார்பனேட், பொட்டாசு என்பதன் முதன்மை கூறு ஆகும். மேலும் சுத்திகரிக்கப்பட்ட முத்து சாம்பல் அல்லது தார் உப்புக்களின் கூறாகவும் உள்ளது. வரலாற்றுரீதியாக, சூளையில் பேக்கிங் பொட்டாசு மூலம் முத்துச்சாம்பல் அசுத்தங்களை நீக்க உருவாக்கப்பட்டது. இறுதியாக கிடைத்த வெள்ளை தூளே முத்துச்சாம்பல் ஆகும். 1790 ல் பாெட்டாசு மற்றும் முத்துச்சாம்பல் உருவாக்கும் முறையை மேம்படுத்தும் காப்புரிமை முதன் முதலாக சாமுவேல் ஆப்கின்சு என்பவருக்கு அமெரிக்க காப்புரிமை அலுவலகத்தால் வழங்கப்பட்டது.
கடந்த 18ம் நூற்றாண்டுகளில் வட அமெரிக்காவில், சமையல் சோடாவின் (பேக்கிங் பவுடர்), வளர்ச்சிக்கு முன்னர் விரைவு ரொட்டிகளில்[2] புளிப்பேற்றிகளாக முத்துச்சாம்பல் பயன்படுத்தப்பட்டது.
தயாரிப்பு
தொகுஇன்று, வணிக ரீதியாக, பாெட்டாசியம் குளோரைடை மின்னாற்பகுப்பதன் மூலம் பாெட்டாசியம் கார்பனேட்டு தயாரிக்கப்படுகிறது. வினையில் உருவான பொட்டாசியம் ஐதராக்சைடு, கரியமில வாயுவினால் கார்பனாக்கம் செய்யப்பட்டு பொட்டாசியம் கார்பனேட்டு தயாரிக்கப்படுகிறது. இது மற்ற பொட்டாசியம் சேர்மங்கள் தயாரிக்க பெருமளவில் பயன்படுத்தப்படுகிறது.
- 2KOH + CO2 → K2CO3 + H2O
பயன்கள்
தொகு- வரலாறுகளில் சோப்பு, கண்ணாடி, மற்றும் சீன பொருட்கள் உற்பத்தி செய்யவும்,
- கால்சியம் குளோரைடு மற்றும் மெக்னீசியம் சல்பேட்டு போன்று மிதமான உலர்த்தும் காரணியாக உள்ளது. இது அமிலச்சேர்மங்களுக்கு ஏற்றதல்ல. சில கீட்டோன்கள், ஆல்ககால் மற்றும் அமீன்களை காய்ச்சிவடித்தலுக்கு[3] முன்னர் உலர்த்தவும் பயன்படுகிறது.
- மதுபானம் தயாரித்தலில் தாங்கல் காரணியாகவும்,
- கடினநீரை[4] மென்னீராக மாற்றவும் பயன்படுகிறது.[சான்று தேவை]
மேற்கோள்கள்
தொகு- ↑ http://chem.sis.nlm.nih.gov/chemidplus/rn/584-08-7
- ↑ See references to "pearl ash" in "American Cookery" by Amelia Simmons, printed by Hudson & Goodwin, Hartford, 1796.
- ↑ Leonard, J.; Lygo, B.; Procter, G. "Advanced Practical Organic Chemistry" 1998, Stanley Thomas Publishers Ltd
- ↑ Child, Lydia M. "The American Frugal Housewife" 1832
நூற்பட்டியல்
தொகுஅறிவியல் அகராதி, ஆக்ஸ்போர்டு யுனிவர்சிட்டி பிரஸ், நியூயார்க், 2004