கால்சியம் குளோரைடு
கல்சியம் குளோரைட்டு (அ) கால்சியம் குளோரைடு (calcium chloride, CaCl2) என்பது கல்சியம் மற்றும் குளோரின் அடங்கிய உப்பு ஆகும். அறைவெப்ப நிலையில் திண்மமாகக் காணப்படுவதுடன் வழமையான அயனி ஆலைடாகவும் நடந்துகொள்ளும். தாவரங்களின் தட்பவெப்ப நிலைகளைப் பேணுவதற்கும், பாதையில் பனி மற்றும் தூசினைக் கட்டுப்படுத்தவும், இது பயன்படுத்தப்படுகிறது. இதன் நீர் உறிஞ்சும் திறனினால், நீரற்ற கால்சியம் குளோரைட்டு, காற்றுப் புகாத கொள்கலனில் அடைத்துப் பாதுகாக்கப்படுகின்றது.

| |
| |
| பெயர்கள் | |
|---|---|
| ஐயூபிஏசி பெயர்
கால்சியம் குளோரைடு
| |
| வேறு பெயர்கள்
கால்சியம் (II) குளோரைடு,
கால்சியம் இரு-குளோரைடு, E509 | |
| இனங்காட்டிகள் | |
| 10043-52-4 | |
| ATC code | A12AA07 B05XA07, G04BA03 |
| ChEBI | CHEBI:3312 |
| ChEMBL | ChEMBL1200668 |
| ChemSpider | 23237 |
| DrugBank | DB01164 |
| EC number | 233-140-8 |
| யேமல் -3D படிமங்கள் | Image |
| பப்கெம் | 24854 |
| வே.ந.வி.ப எண் | EV9800000 |
SMILES
| |
| UNII | OFM21057LP |
| பண்புகள் | |
| CaCl2 | |
| வாய்ப்பாட்டு எடை | 110.98 கி/மோல் (நீரிலி) 128.999 கி/மோல் (ஒற்றைநீரேறி) 147.014 கி/மோல் (இருநீரேறி) 183.045 கி/மோல் (நான்குநீரேறி) 219.08 கி/மோல் (ஆறுநீரேறி) |
| தோற்றம் | வெண்ணிற பொடி நீர் உறிஞ்சி |
| மணம் | மணமற்றது |
| அடர்த்தி | 2.15 கி/செமீ3 (நீரிலி) 1.835 கி/செமீ3 (இருநீரேறி) 1.83 கி/செமீ3 (நான்குநீரேறி) 1.71 கி/செமீ3 (ஆறுநீரேறி) |
| உருகுநிலை | 772 °செ (நீரிலி) 260 °செ (ஒற்றைநீரேறி) 176 °செ (இருநீரேறி) 45.5 °செ (நான்குநீரேறி) 30 °செ (ஆறுநீரேறி)[1] |
| கொதிநிலை | 1935 °C (நீரிலி) |
| 74.5 கி/100 மிலி (20 °செ) 59.5 கி/100 மிலி (0 °செ) | |
| கரைதிறன் | அசெட்டோன், அசெடிக் அமிலம் |
| காடித்தன்மை எண் (pKa) | 8–9 (நீரிலி) 6.5–8.0 (ஆறுநீரேறி) |
| ஒளிவிலகல் சுட்டெண் (nD) | 1.52 |
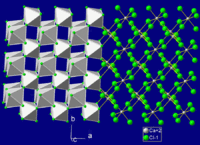
| கட்டமைப்பு | |
| படிக அமைப்பு | செஞ்சாய் சதுரம் (சிதைந்த வடிவம் இரூட்டைல்), oP6 முக்கோணம் (ஆறுநீரேறி) |
| புறவெளித் தொகுதி | Pnnm, No. 58 |
| ஒருங்கிணைவு வடிவியல் |
எண்முகமானது, 6-ஆயங்கள் |
| தீங்குகள் | |
| GHS pictograms | 
|
| H319, H316, H302 | |
| P264, P280, P270, P305+351+338, P337+313, P301+312, P330, P501 | |
| ஈயூ வகைப்பாடு | Irritant (Xi) |
| R-சொற்றொடர்கள் | R36 |
| S-சொற்றொடர்கள் | (S2), S22, S24 |
| Lethal dose or concentration (LD, LC): | |
LD50 (Median dose)
|
1000 mg/kg (oral, rat) |
| தொடர்புடைய சேர்மங்கள் | |
| ஏனைய எதிர் மின்னயனிகள் | கால்சியம் ஃபுளோரைடு கால்சியம் புரோமைடு கால்சியம் அயோடைடு |
| ஏனைய நேர் மின்அயனிகள் | பெரிலியம் குளோரைடு மெக்னீசியம் குளோரைடு துரந்தியம் குளோரைடு பேரியம் குளோரைடு ரேடியம் குளோரைடு |
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |
| | |
| Infobox references | |
பண்புகள் தொகு
கல்சியம் குளோரைடு தண்ணீரில் கரைதிறனைக் கொண்டிருப்பதால், கல்சியம் அயனி, கரைசலை உருவாக்கிட மூலப்பொருளாகப் பயன்படுகிறது. இப்பண்பினால் கரைசல்களில் இருந்து அயனிகளைப் பிரித்தெடுக்க இது பயன்படுத்தப்படுகிறது. எடுத்துக்காட்டாக, கல்சியமினால், கரைசலில் இருந்து பாஸ்பேட்டின் இட மாற்றம்:
3 CaCl2 (aq) + 2 K3PO4 (aq) → Ca3(PO4)2 (s) + 6 KCl (aq)
உருகிய கல்சியம் குளோரைட்டை மின் பகுப்பு மூலம், கல்சியம் திண்மத்தையும், குளோரின் வாயுவினையும் பெறல்:
CaCl2 (l) → Ca (s) + Cl2 (g)
கல்சியம் குளோரைடு, கரைசலில் உயர்வான வெப்ப அடக்க (enthalpy change of solution) மாற்றத்தினைக் கொண்டுள்ளது. தண்ணீரில் கரைசலை உண்டாக்கும் போது கணிசமான வெப்ப உயர்வு ஏற்படும்.
நீரற்ற உப்பான இது, நீர் உறிஞ்சியாக இருக்கும். கரைசல் நிலைக்கு மாற்றமடைய, பெருமளவான நீரினைத் தன் படிக அமைப்பினுள் உறிஞ்சிக் கொள்ளும்.
உற்பத்தி தொகு
கல்சியம் குளோரைடினைச் சுண்ணக்கல்லில் இருந்து நேரடியாக உற்பத்தி செய்ய முடியும். இருந்தாலும் அது பெருமளவில் சொல்வே செயல்முறை (solvay process) மூலமே செய்யப்படுகிறது. 2002 ம் ஆண்டு வட அமெரிக்காவின் நுகர்வு 1,687,000 டன்களாக (3.7 பில்லியன் பவுண்டுகள்)[2] இருந்தது. அமெரிக்காவின் மொத்த கல்சியம் குளோரைட்டு உற்பத்தியில், 35% இனை டொவ் கெமிக்கல் நிறுவனம் (Dow Chemical Company) உற்பத்தி செய்கிறது[3].
பயன்கள் தொகு
ஈரமுறிஞ்சி தொகு
உலர்த்தும் குழாய்கள் பெரும்பாலும் கல்சியம் குளோரைடைக் கொண்டே நிரப்பப்பட்டிருக்கும். சோடியம் காபனேற்றுவின் உற்பத்தியில் பயன்படும் ஒரு வகைக் கடல் பாசி (kelp) வகையிலிருந்து நீரினை அகற்றப் பாவிக்கப்படும். கரைசல்களுக்குத் திண்மக் கல்சியம் குளோரைடைச் சேர்ப்பதினால் நீரினை அகற்றலாம். நீரற்றக் கல்சியம் குளோரைடை, நீர் உறிஞ்சியாகப் (ஈரமற்ற தன்மையை உறுதிப்படுத்த) பயன்படுத்தலாம் என அமெரிக்க உணவு மற்றும் மருந்து நிர்வாகம் அனுமதித்துள்ளது (CPG 7117.02).[4]
இதன் நீர் உறிஞ்சும் திறன் பாதையில் திரவ அடுக்கினை உருவாக்கி, தூசினைக் கட்டுப்படுத்தவும் பயன்படுகிறது[5].
பனி நீக்கம் மற்றும் உறைநிலை அமுக்கம் தொகு
கல்சியம் குளோரைடு, நீரின் உறைநிலை அமுக்கத்தைக் குறைப்பதன் மூலம், பனி உருவாகுவதை தடுக்கவும், பனியை நீக்கவும் உதவுகிறது. இது பாதை மேற்பரப்புகளிலிருந்து பனியை நீக்க உதவியாய் உள்ளது. கல்சியம் குளோரைடு கரைசல் நிலையை அடையும் போது வெப்பத்தினை உமிழும், எனினும் சுற்றியுள்ள தாவரங்களுக்கும், மண்ணிற்கும், ஒப்பிட்ட அளவில் பாதிப்பு ஏற்படுத்தாததாய் உள்ளது; இருந்த போதும், வாஷிங்டன் மாநிலம், பாதையோர பசுமைத் தாவரங்களுக்கு கால்சியம் குளோரைடு பாதிப்பை ஏற்படுத்தக்கூடும் என பரிந்துரைத்துள்ளது[6]. குறைந்த வெப்ப நிலையில் சோடியம் குளோரைடினை விட அதிக பயனுள்ளது. மிகவும் சிறிய அளவான வெள்ளை நிற குளிகைகளாக கால்சியம் குளோரைடு பயன்படுத்தப்படுகின்றது.
கல்சியம் அயனிகளின் மூலம் தொகு
நீச்சல் தடாகங்களில் நீரின் கடினத்தன்மையை அதிகரிக்க கல்சியம் குளோரைடு பயன்படுத்தப்படுகிறது. இது தடாக சுவர்களில் ஏற்படும் அரிப்பினை தடுக்கும். லீ சாட்லியர் தத்துவம், பொது அயனி விளைவுகளுக்கு ஏற்ப, நீரில் கல்சியத்தின் செறிவு அதிகரிக்கும் பொழுது, தடாக கல்சியம் கலவைக் கட்டிடப் பகுதியில் ஏற்படும் அரிப்பு குறைவடையும்.
நீர்வாழ் உயிரினங்கள் காட்சிச்சாலையில், மெல்லுடலி, நிடேரியா போன்ற உயிரினங்கள் வாழ்வதற்கான ஊடகத்தை அமைக்க கல்சியம் குளோரைடு சேர்க்கப்படுகிறது. கல்சியம் ஐதரொக்சைடு அல்லது கால்சியம் உலை, கல்சியமினை அறிமுகப்படுத்த பயன்படுத்தப்படலாம், இருந்தாலும் கல்சியம் குளோரைடின் சேர்க்கை வேகமானதாக இருப்பதுடன், காரகாடித்தன்மைச் சுட்டெண்ணிலும் குறைவான தாக்கத்தையே செலுத்துகின்றது.
உணவு தொகு
ஐரோப்பிய ஒன்றியம் உணவினை சுவையூட்டும், உணவு மூலப்பொருளாக, ஈ-இலக்கம் (E number) E509 கீழ் அனுமதி அளித்துள்ளது. அமெரிக்க உணவு மற்றும் மருந்துகள் நிர்வாகத்தின், உணவில் சேர்க்க பாதுகாப்பனது (Generally recognized as safe (GRAS)) எனும் பகுதிக்குள் அனுமதிக்கப்பட்டுள்ளது[7]. அதனுடன், அமெரிக்க தேசிய கரிம திட்டங்கள் (National Organic Program) குழுவின், தேசியப்பட்டியலான அனுமதிக்கப்பட்ட மற்றும் புறக்கணிக்கப்பட்ட பொருட்களிலும் இணைக்கப்பட்டுள்ளது[8]. தனிமனிதனுக்கு சராசரியாக ஒரு நாளைக்கு 160–345 மி.கி. என்ற அளவில் உணவில் கல்சியம் குளோரைட்டினை சேர்த்துக் கொள்ள அனுமதி அளிக்கப்பட்டுள்ளது[9].
கல்சியம் குளோரைடு பதப்படுத்தும் பொருளாக, பேணிகளில் அடைக்கப்பட்ட மரக்கறிகளில், சோயா அவரை தயிர் ஆனா டோஃபூ தயாரிப்பு என்பவற்றில் பாவிக்கப்படுகிறது[10]. போத்தலில் அடைக்கப்பட்ட குடிநீர் உள்ளடங்கலாக விளையாட்டு பானங்களிலும், மற்றைய பானங்களிலும் மின்பகுளியாக பொதுவாக பயன்படுத்தப்படுகிறது. கடும் உப்புச்சுவையுடைய கல்சியம் குளோரைட்டு, உணவிலிருக்கும் சோடியமின் அளவினை அதிகரிக்காது சுவையூட்ட பயன்படுகிறது. கல்சியம் குளோரைட்டின் உறை நிலை அமுக்கம். எரிசர்க்கரை (caramel) நிரப்பப்பட்ட இன்னட்டு (சொக்கலேட்) கட்டிகளில், எரிசர்க்கரை உறையாமல் இருக்க பயன்படுகிறது.
நொதியாதல் (brewing) முறை பீர் தயாரிப்பில் சில சந்தர்ப்பங்களில், நொதியாகும் நீரில் இருக்கும் கனிம குறைவினை நிவர்த்தி செய்ய பயன்படுத்தப்படுகிறது. இது நொதியாதல் செயன்முறையின் போது சுவை மற்றும் இரசாயன மாற்றத்தில் தாக்கத்தை செலுத்துவதோடு, நுரைமத்தினை (yeast) நொதிக்கச் செய்யும் செயன்முறையிலும் தாக்கத்தை செலுத்துகிறது. பாலாடைக்கட்டி (cheese) செய்யும் பொழுது கல்சியத்திற்கும், புரதத்திற்கும் இடையேயான சமச்சீர் தன்மையை பேணுவதற்காக பதப்படுத்தப்பட்ட பாலில் சேர்க்கப்படுகிறது.
மருந்து தொகு
உள்ளக ஐட்ரோ புளோரிக் அமில எரிவிற்கு சிகிச்சையாக ஊசி மூலம் ஏற்றப்படும். மக்னீசியம் நஞ்சினை குணமாக்க பயன்படுத்தப்படும். இதய துடிப்பலைஅளவி கணிப்பீட்டின் படி,கல்சியம் குளோரைட்டு ஊசி இதயம் சம்மந்தமான நச்சுத்தன்மைக்கு எதிரானதாக உள்ளது. இரத்த மிகைப்பொட்டாசிய அளவில் (Hyperkalemia) காணப்படும் அபாயகரமான உயர்ந்த அளவான பொட்டாசியத்தில் இருந்து இதயத்தசையினைப் பாதுகாக்க உதவும். பக்கவிளைவுகளால் உருவான, கல்சியத்தின் பரவலை தடுக்கும் நச்சுப் பொருட்களுக்கு துரித நிவாரனியாக பயன்படுத்தப்படும், மாரடைப்பினை தவிர்க்க உதவிசெய்கின்றது.[11]
வாய் வழியாகவோ அல்லது நரம்பு வழியாகவோ கல்சியம் குளோரைட்டினை உள்ளெடுக்கும் போது பக்கவிளைவுகள் ஏற்படுவதற்கான வாய்ப்புகள் காணப்படுகின்றன. பின்வரும் நிலைமைகளினால் பாதிக்கப்பட்டிருப்பவர்களுக்கு கல்சியம் குளோரைட்டினை உள்ளெடுத்தல் பரிந்துரைக்கப்படவில்லை :
- கல்சியம் உப்புடன் ஒவ்வாமை உடையவர்கள்
- இதயப் பிரச்சனைக்கு மருந்து உட்கொள்பவர்கள்
- சிறுநீரகப் பிரச்சனைகளால் குறைந்த கல்சியம் மட்டத்தினை பேணுபவர்கள்
- இரத்தத்திலோ, சிறுநீரிலோ அதிகளவான கல்சியம் மட்டத்தினை கொண்டிருப்பவர்கள்
- மூச்செடுப்பதில் பிரச்சனை உள்ளவர்கள்
கல்சியம் குளோரைட்டினை உள்ளெடுப்பதில் சிறப்பு கவனம் எடுக்க வேண்டியவர்கள் :
விலங்குக் கருத்தடை தொகு
எதனோலுடன், நிறையில் 20 சதவிகிதம் கலக்கப்பட்ட கல்சியம் குளோரைட்டு, ஆண் விலங்குகளுக்கு கருத்தடையினை ஏற்படுத்த பயன்படுத்தப்படும். அறுவைச் சிகிச்சையற்ற முறையில், ஆண் விலங்கின் விரையில் ஊசி மூலம் கரைசல் ஏற்றப்படும். ஒரு மாதத்தினுள், விதை திசுவில் உள்ள இழைமங்களின் அழிவு கருத்தடையினை உறுதிப்படுத்தும்[13][14].
மற்றவை தொகு
கல்சியம் குளோரைடு, ஆரம்ப செயற்பாட்டினை துரிதப்படுத்துவதற்காக காங்கிறீற்று கலவைகளில் கலக்கப்படும், எனினும் குளோரைடு அயனி இரும்பு (Rebar) அரிப்பை அதிகப்படுத்தும். எனவே, இது வலுவூட்டப்பட்ட காங்கிறீற்று கலவையில் பயன்படுத்தப்படுவதில்லை[15]. நீரற்ற கல்சியம் குளோரைட்டு, ஈரமற்ற காங்கிறீற்றினை உறுதிப்படுத்த அளவுகோலாக பயன்படுகிறது[16].
கல்சியம் குளோரைடானது நீச்சல் தடாகத்தில் நீரின் காரகாடித்தன்மைச் சுட்டெண் அளவினை பேணுவதற்கும், நீரில் கல்சியத்தின் செறிவினை பேணுவதற்கும் பயன்படுகிறது. கல்சியம் குளோரைடின் வெப்பம் உமிழும் தன்மை, சுய சூடேற்றும் தகரக் குவளைகளிலும் (cans), சூடாக்கும் திண்டுகளிலும் (pad) பயன்படுத்தப்படுகிறது.
எண்ணெய்த் தொழில்துறையில், திண்மமற்ற உப்புநீரின் (brines) அடர்த்தியை அதிகரிக்க பயன்படுகிறது. சோடியம் உலோகத் தயாரிப்பின் பகுதியான, டேவி (Davy) செயல்முறையின் பொழுது உருகிய சோடியம் குளோரைடுடனான மின்பகுப்பின் போது பயன்படுத்தப்படுகிறது. மேலும், பீங்கான் பொருள் தயாரிப்பிலும் ஒரு மூலப்பொருளாக பயன்படுகிறது.
இடையூறுகள் தொகு
கல்சியம் குளோரைடு ஈரமான தோலில் எரிச்சல் தன்மையினை ஏற்படுத்தும். திண்ம கல்சியம் குளோரைடு வெப்பம் விடு வினையை கொண்டிருப்பதால், அதனை உட்கொள்ளும் பொழுது வாய் மற்றும் உணவுக்குழாய் பகுதிகளில் தீப்புண்களை உண்டாக்கும். செறிவாக்கப்பட்ட கரைசலை உள்ளெடுக்கும் பொழுது அல்லது திண்மப்பொருளாக உள்ளெடுக்கும் பொழுது இரைப்பையில் எரிச்சலையோ அல்லது புண்ணையோ ஏற்படுத்தும்[17].
கல்சியம் குளோரைடினை பாவிப்பதனால் ஏற்படக்கூடிய வேறு சில பக்க விளைவுகள் :
- வாயினுள் சுண்ண (chalky) சுவை ஏற்படல்
- தசை சூடாதல்
- குறைவான இரத்த அழுத்தம்
- பசி ஏற்படாதிருத்தல்
- காய்ச்சலாக உணர்தல்
- வாந்தி மயக்கம்
- மலச்சிக்கல்
- வயிற்று வலி
- பலவீனமாக உணர்தல்
- மனக்குழப்பம்
- அதிகமான தாகம்
- அதிகளவான சிறுநீர் கழித்தல்
- எலும்பு வலி
- சிறுநீரகத்தில் கல்சியம் வீழ்படிதல்
- சிறுநீரக கல்
- அசாதாரணமான இதயத்துடிப்பு
- உணர்விழந்த நிலை
இவற்றில் ஏதேனும் ஒரு அறிகுறி இரத்தத்தில் தென்பட்டால் கல்சியத்தின் மட்டம் அதிகமாக உள்ளதைக் குறிக்கும்[18].
கல்சியம் குளோரைடு உப்பு சிறிய அளவில் உலோகத்தன்மையை (அலுமினியம்) கொண்டிருக்கும், ஆகவே அதிகளவான கல்சியம் குளோரைடு பாவனை நஞ்சுத்தன்மையை ஏற்படுத்தும்.
மேற்கோள்கள் தொகு
- ↑ Pradyot Patnaik. Handbook of Inorganic Chemicals. McGraw-Hill, 2002, பன்னாட்டுத் தரப்புத்தக எண் 0-07-049439-8
- ↑ Calcium Chloride SIDS Initial Assessment Profile, UNEP Publications, SIAM 15, Boston, 22–25 October 2002, page 11.
- ↑ Calcium Chloride Chemical Profile, The Innovation Group, www.the-innovation-group.com, printed 9 September 2005.
- ↑ "CPG 7117.02". FDA Compliance Articles. US Food and Drug Administration. March 1995. பார்க்கப்பட்ட நாள் 3 December 2007.
- ↑ "Dust: Don't Eat It! Control It!". Road Management & Engineering Journal. US Roads (TranSafety Inc.). 1 June 1998. Archived from the original on 29 October 2007. பார்க்கப்பட்ட நாள் 9 August 2006.
- ↑ "De-icer damaging thousands of trees on mountain passes". The Seattle Times. 19 March 2008. பார்க்கப்பட்ட நாள் 18 March 2008.
- ↑ 21 CFR § 184.1193
- ↑ 7 CFR § 205.602
- ↑ Calcium Chloride SIDS Initial Assessment Profile, UNEP Publications, SIAM 15, Boston, 22–25 October 2002, pp. 13–14.
- ↑ "Apple Caviar Technique". StarChefs Studio. StarChefs.com. April 2004. பார்க்கப்பட்ட நாள் 9 August 2006.
- ↑ "Calcium chloride Prescribing Information". Hospira, Inc. November 2009. Archived from the original on 21 March 2012. பார்க்கப்பட்ட நாள் 10 June 2011.
- ↑ http://www.drugs.com/pro/calcium-chloride.html பரணிடப்பட்டது 2012-02-06 at the வந்தவழி இயந்திரம் | title = Calcium Chloride Intravenous Infusion
- ↑ Koger, Nov 1977, "Calcium Chloride, Practical Necrotizing Agent", Journal of the American Association of Bovine Practitioners (USA), (Nov 1977), v. 12, p. 118–119
- ↑ Jana, K.; Samanta, P. K.. "Clinical evaluation of non-surgical sterilization of male cats with single intra-testicular injection of calcium chloride". BMC Vet Res.. doi:10.1186/1746-6148-7-39. பப்மெட்:21774835.
- ↑ "Accelerating Concrete Set Time". Federal Highway Administration. 1 June 1999. Archived from the original on 17 சனவரி 2007. பார்க்கப்பட்ட நாள் 16 January 2007.
- ↑ National Research Council (U.S.). Building Research Institute (1962). Adhesives in Building: Selection and Field Application; Pressure-sensitive Tapes. National Academy of Science-National Research Council. பக். 24–5.
- ↑ "Product Safety Assessment (PSA): Calcium Chloride". டொவ் கெமிக்கல் கம்பனி. 2 May 2006.
- ↑ url = http://www.drugs.com/pro/calcium-chloride.html பரணிடப்பட்டது 2012-02-06 at the வந்தவழி இயந்திரம் | title = Calcium Chloride Possible Side Affects