குளோரின் ஒருபுளோரைடு
குளோரின் ஒருபுளோரைடு(Chlorine monofluoride) என்பது ClF என்ற மூலக்கூற்று வாய்பாடு கொண்ட ஒரு கனிம வேதியியல் சேர்மமாகும்.குளோரின் மோனோபுளோரைடு என்ற பெயராலும் இச்சேர்மம் அழைக்கப்படுகிறது. அறை வெப்பநிலையில் நிறமற்ற வாயுவாகக் காணப்படும் இது உயர் வெப்பநிலையிலும் கூட நிலைப்புத்தன்மையுடன் காணப்படுகிறது. -100 பாகை செல்சியசு வெப்பநிலைக்கு குளிர்விக்கும்போது குளோரின் ஒருபுளோரைடு வெளிறிய மஞ்சள்நிற திரவமாகக் குறுக்கமடைகிறது. இதனுடைய பல பண்புகள் மூல ஆலசன்களான அல்லது உப்பீனிகளான குளோரின் மற்றும் புளோரின் ஆகியனவற்றிற்கு இடைப்பட்ட நிலையில் உள்ளது.[1]
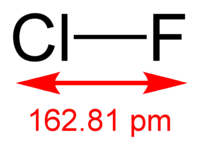
| |

| |
| பெயர்கள் | |
|---|---|
| ஐயூபிஏசி பெயர்
குளோரின் ஒருபுளோரைடு
| |
| வேறு பெயர்கள்
குளோரின் புளோரைடு
| |
| இனங்காட்டிகள் | |
| 7790-89-8 | |
| ChemSpider | 109879 |
InChI
| |
| யேமல் -3D படிமங்கள் | Image |
| பப்கெம் | 123266 |
| |
| பண்புகள் | |
| ClF | |
| வாய்ப்பாட்டு எடை | 54.45 கி/மோல் |
| அடர்த்தி | 1.62 கி.மி.லி (திரவம், −100 °செ) |
| உருகுநிலை | −155.6 °C (−248.1 °F; 117.5 K) |
| கொதிநிலை | −100.1 °C (−148.2 °F; 173.1 K) |
| கட்டமைப்பு | |
| இருமுனைத் திருப்புமை (Dipole moment) | 0.881 D (2.94 × 10−30 C m) |
| வெப்பவேதியியல் | |
| Std enthalpy of formation ΔfH |
−56.5 kJ mol−1 |
| நியம மோலார் எந்திரோப்பி S |
217.91 J K−1 mol−1 |
| வெப்பக் கொண்மை, C | 33.01 J K−1 mol−1 |
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |
வினைகள்
தொகுகுளோரின் ஒருபுளோரைடு ஒரு பல்தி்றமிக்க புளோரினேற்றும் செயலியாக விளங்குகிறது. உலோகங்களையும் அலோகங்களையும் அவற்றின் புளோரைடுகளாக மாற்றி குளோரின் வாயுவையும் அச்செயல்முறையின் விளைவாக வெளியிடுகிறது. உதாரணமாக தங்குதனை தங்குதன் அறுபுளோரைடாகவும், செலினியத்தை செலினியம் நான்மபுளோரைடாகவும் மாற்றுகிறது.
- W + 6 ClF → WF6 + 3 Cl2
- Se + 4 ClF → SeF4 + 2 Cl2
பல பிணைப்புகளாக கூட்டு வினையின் மூலம் அல்லது ஆக்சிசனேற்ற வினையின் மூலம் சேர்மங்களை இச்சேர்மம் குளோரோபுளோரினேற்றமும் செய்கிறது. உதாரணமாக கார்பன் ஓராக்சைட்டில் உள்ள முப்பிணைப்பில் புளோரினையும் குளோரினையும் சேர்த்துவிடுகிறது.
மேற்கோள்கள்
தொகு- ↑ Otto Ruff, E. Ascher (1928). "Über ein neues Chlorfluorid-CIF3". Zeitschrift für anorganische und allgemeine Chemie 176 (1): 258–270. doi:10.1002/zaac.19281760121.
இவற்றையும் காண்க
தொகுவெளி இணைப்புகள்
தொகு- National Pollutant Inventory - Fluoride and compounds fact sheet பரணிடப்பட்டது 2006-01-16 at the வந்தவழி இயந்திரம்
- WebBook page for ClF