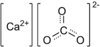கால்சியம் கார்பனேட்டு
கால்சியம் கார்பனேட்டு (CaCO3) என்ற மூலக்கூறு வாய்ப்பாட்டைக் கொண்டுள்ள வேதிச்சோ்மம் ஆகும். இது பாறைகளில் காணப்படும் கனிமங்களான கால்சைட்டு மற்றும் அரகோனைட்டு (இந்த இரண்டு கனிமங்களையும் கொண்டுள்ள சுண்ணாம்புக்கல்) ஆகியவற்றில் காணப்படும் ஒரு பொதுப்பொருளாகும். இது முத்துக்கள், கடல் வாழ் உயிாினங்கள், நத்தைகள் மற்றும் முட்டைகளின் ஓடுகள் இவற்றில் காணப்படும் முதன்மைப் பகுதிப்பொருள் ஆகும். மருத்துவத்துறையில் இது ஒரு வயிற்றில் உள்ள புளிப்புத் தன்மையை மாற்றும் பொருளாகவும், கால்சியத்திற்கான உப உணவுப்பொருளாகவும் பயன்படுத்தப்படுகிறது. இருப்பினும் இப்பொருளின் அதிகமான பயன்பாடு ஆபத்தை விளைவிக்கலாம்.
| |||

| |||
| பெயர்கள் | |||
|---|---|---|---|
| ஐயூபிஏசி பெயர்
கால்சியம் கார்பனேட்டு
| |||
| வேறு பெயர்கள் | |||
| இனங்காட்டிகள் | |||
| 471-34-1 | |||
| ChEBI | CHEBI:3311 | ||
| ChEMBL | ChEMBL1200539 | ||
| ChemSpider | 9708 | ||
| EC number | 207-439-9 | ||
| யேமல் -3D படிமங்கள் | Image Image | ||
| KEGG | D00932 | ||
| பப்கெம் | 10112 | ||
| வே.ந.வி.ப எண் | FF9335000 | ||
| |||
| UNII | H0G9379FGK | ||
| பண்புகள் | |||
| CaCO3 | |||
| வாய்ப்பாட்டு எடை | 100.0869 கி/மோல் | ||
| தோற்றம் | வெண்ணிற நுண்ணியத் துாள்; சுண்ணாம்புச் சுவை | ||
| மணம் | மணமற்றது | ||
| அடர்த்தி | 2.711 கி/செமீ3 (கால்சைட்டு) 2.83 g/cm3 (அரகோனைட்டு) | ||
| உருகுநிலை | 1,339 °C (2,442 °F; 1,612 K) (calcite) 825 °C (1517 °F; 1,098 K) (aragonite) [1] | ||
| கொதிநிலை | சிதைவுறுகிறது | ||
| 0.013 கி/லி (25 °செ)[2][3] | |||
கரைதிறன் பெருக்கம் (Ksp)
|
3.3×10-9[4] | ||
| நீர்த்த அமிலங்கள்-இல் கரைதிறன் | கரையக்கூடியது | ||
| காடித்தன்மை எண் (pKa) | 9.0 | ||
| -38.2·10−6 செமீ3/மோல் | |||
| ஒளிவிலகல் சுட்டெண் (nD) | 1.59 | ||
| கட்டமைப்பு | |||
| படிக அமைப்பு | முக்கோணம் | ||
| புறவெளித் தொகுதி | 32/m | ||
| வெப்பவேதியியல் | |||
| Std enthalpy of formation ΔfH |
−1207 kJ·mol−1[5] | ||
| நியம மோலார் எந்திரோப்பி S |
93 J·mol−1·K−1[5] | ||
| தீங்குகள் | |||
| பொருள் பாதுகாப்பு குறிப்பு தாள் | ICSC 1193 | ||
| தீப்பற்றும் வெப்பநிலை | 825 °C (1,517 °F; 1,098 K) | ||
| Lethal dose or concentration (LD, LC): | |||
LD50 (Median dose)
|
6450 மிகி/கிகி (வாய்வழி, எலி) | ||
| அமெரிக்க சுகாதார ஏற்பு வரம்புகள்: | |||
அனுமதிக்கத்தக்க வரம்பு
|
TWA 15 மிகி/மீ3 (total) TWA 5 மிகி/மீ3 (resp)[6] | ||
| தொடர்புடைய சேர்மங்கள் | |||
| ஏனைய எதிர் மின்னயனிகள் | Calcium bicarbonate | ||
| ஏனைய நேர் மின்அயனிகள் | மக்னீசியம் கார்பனேட்டு இசுட்ரான்சியம் கார்படே்டு பேரியம் கார்பனேட்டு | ||
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |||
கால்சியம் கார்பனேட்டின் வேதிப்பண்புகள்
தொகுகால்சியம் கார்பனேட்டு உப்புக்களுக்கான பொதுவான வினைகளைத் தருகின்றது. அமிலங்களுடன் வினைபுரிந்து கார்பன் டை ஆக்சைடை வெளிவிடுகிறது.
CaCO3(திண்மம்) + 2H+(நீா்த்த) → Ca2+(நீா்த்த) + CO2(வாயு) + H2O (திரவம்)
வெப்பத்தால் இச்சேர்மம் சிதைவடைந்து சுட்ட சுண்ணாம்பு மற்றும் கார்பன் டை ஆக்சைடைத் தருகிறது. இந்த வினை வெப்பச்சிதைவு அல்லது கால்சினேஷன் என அழைக்கப்படுகிறது.
CaCO3 (திண்மம்) → CaO (திண்மம்) + CO2 (வாயு)
கால்சியம் கார்பனேட்டானது கார்பன் டை ஆக்சைடினால் பூரிதமாக்கப்பட்ட நீருடன் வினைபுரிந்து நீரில் கரையக்கூடிய கால்சியம் பை கார்பனேட்டைத் தருகிறது.
CaCO3 + CO2 + H2O → Ca(HCO3)2
இந்த வினையானது கார்பனேட்டு பாறைகளின் அரிமானத்திற்கு காரணமான ஒரு வினையாக உள்ளது. இந்த வினையே நிலக்குடைவுகளிலிருந்து கால்சியம் உப்புக்களைக் கரைத்து நீரைக் கடினத்தன்மையுடையதாக மாற்றுகின்றது.
தயாாிப்பு
தொகுதொழிற்துறையில் பயன்படுத்தப்படும் மிகப்பெரும்பகுதி கால்சியம் கார்பனேட்டானது சுரங்கவியல் மற்றும் பாறைகள் வெட்டியெடுத்தல் முறையில் பெறப்படுபவையே ஆகும். உணவு மற்றும் மருத்துவத்துறை தேவைகளுக்கான தூய்மையான கால்சியம் கார்பனேட்டானது சுரங்கங்களிலிருந்து பெறப்படும் தூய கனிமங்களிலிருந்து (பெரும்பாலும் - பளிங்குக்கல்) தயாரிக்கப்படுகின்றது.
மாற்று முறையாக, கால்சியம் கார்பனேட்டானது கால்சியம் ஆக்சைடில் இருந்து தயாரிக்கப்படுகிறது. கால்சியம் ஆக்சைடுடன் நீர் சேர்க்கப்படும் போது, கால்சியம் ஐட்ராக்சைடு கிடைக்கிறது. அவ்வாறு கிடைக்கும் கால்சியம் ஐட்ராக்சிடுனுள் கார்பன் டை ஆக்சைடு வாயுவானது செலுத்தப்படுகிறது. இதன் காரணமாக வீழ்படிவாக்கப்பட்ட தேவையான கால்சியம் கார்பனேட்டு கிடைக்கிறது. இவ்வாறு கிடைக்கும் கால்சியம் கார்பனேட்டானது தொழிற்துறையில் வீழ்படிவாக்கப்பட்ட கால்சியம் கார்பனேட்டு (PCC-Precipitated Calcium Carbonate)[7] என அழைக்கப்படுகிறது.
- CaO + H2O → Ca(OH)2
அமைப்பு
தொகுவெப்ப இயக்கவியல் ரீதியாக இயல்பான நிலைகளில் β-CaCO3 (கால்சைட்டு கனிமம்) நிலையானதாக இருக்கிறது. மற்ற வடிவங்களான நேர்சாய்சதுர (orthorhombic) λ-CaCO3(அரகோனைட்டு கனிமத்தில் காணப்படுவது), μ-CaCO3(வேடரைட் கனிமத்தில் காணப்படுவது) ஆகியவை தயாரிக்கப்படலாம். அரகோனைட்டு வடிவத்தை 85 °C வெப்பநிலைக்கு அதிகமான நிலையில் வீழ்படிவாக்குதலாலும், வேடரைட் வடிவத்தை 60 °C வெப்பநிலையில் வீழ்படிவாக்குதலாலும் தயாரிக்க முடியும். கால்சைட்டானது 6 ஆக்சிஜன் அணுக்களால் சூழப்பட்ட கால்சியம் அணுவையும், அரகோனைட்டானது 8 ஆக்சிஜன் அணுக்களால் சூழப்பட்ட கால்சியம் அணுவையும் கொண்டுள்ளது வேடரைட் வடிவத்தின் அமைப்பானது முற்றிலும் அறியப்படவில்லை.
இயற்கையில் காணப்படும் விதங்கள்
தொகுநிலவியல் மூலங்கள்
தொகுகால்சைட்டு, அரகோனைட்டு, வேடரைட்டு ஆகியவை கால்சியம் கார்பனேட்டின் தூய கனிமங்கள். தொழிற்துறையில் அதிக அளவில் பயன்படுத்தப்படும் பாறைக் கனிமங்கள் சுண்ணாம்புக்கல், சுண்ணாம்பு, பளிங்குக்கல், டிராவெர்டைன் ஆகியவையாகும்.
உயிரியல் சார்ந்த மூலங்கள்
தொகுபெரும்பான்மையான கடல் வாழ் உயிரினங்களின் ஓடுகள், நத்தைகளின் ஓடுகள், முட்டைகளின் கூடுகள் அதிக அளவில் கால்சியம் கார்பனேட்டைக் கொண்டுள்ளதால் தொழிற்துறைக்கான கால்சியம் கார்பனேட் மூலங்களாக பயன்படுகின்றன. சிப்பிகள் அல்லது கிளிஞ்சல்கள் சமீபத்தில் உணவுக்கான கால்சியம் கார்பனேட்டின் மூலங்களாக அங்கீகாிக்கப்பட்டுள்ளன. இவை நடைமுறை தொழில் துறை மூலங்களாகவும் உள்ளன. அடர் பச்சை நிறமுடைய காய்கறிகளான பிராக்கோலி மற்றும் காலே என அழைக்கப்படும் முட்டைக்கோசு வகைத் தாவரம் இவைகளில் அதிக கால்சியம் கார்பனேட்டு உள்ளது. ஆனால், இவற்றை தொழிற்துறை மூலங்களாக பயன்படுத்த இயலாது.
புவிக்கப்பாலான மூலங்கள்
தொகுபுவிக்கு அப்பாலும் கால்சியம் கார்பனேட்டின் மூலங்கள் காணப்படுகின்றன. மிகவும் நம்பத்தகுந்த சான்றுகள் செவ்வாய் கோளில் கால்சியம் கார்பனேட்டின் இருப்பை உறுதிப்படுத்துகின்றன. செவ்வாய் கோளில் ஒன்றுக்கும் மேற்பட்ட இடங்களில் (குறிப்பாக குசேவ் மற்றும் ஹைஜென்ஸ் பள்ளங்களில்), இதுவே கடந்த காலங்களில் செவ்வாய் கோளில் திரவ வடிவிலான நீர் இருந்தமைக்கான சான்றாக இருக்கிறது.
பயன்கள்
தொகு- கட்டுமானத் துறையில் பயன்படுத்தப்படுவது கால்சியம் கார்பனேட்டின் முக்கிய பயன்பாடாகும். ஒரு கட்டுமானப் பொருளாக அல்லது சாலை கட்டுமானத்திற்கான சுண்ணாம்பு குழம்பாக அல்லது ஒரு சிமெண்ட் கலவையின் பகுதிப் பொருளாக அல்லது ஒரு சூளையை எரியச் செய்யும் தொடக்கப் பொருளாக என பல்வேறு வகைகளில் கால்சியம் கார்பனேட்டு பயன்படுகிறது. கால்சியம் கார்பனேட் சுண்ணாம்பு வடிவில் தற்போது பயன்படுத்தப்படுவதில்லை, ஆனால் கட்டுமான பொருட்களுக்கான ஒரு மூல / முதன்மை பொருளாக மட்டுமே பயன்படுத்தப்படுகிறது.
- கால்சியம் கார்பனேட்டு ஊது உலையில் இரும்புத் தாதுவிலிருந்து இரும்பைப் பிரித்தெடுக்க உதவுகிறது. கால்சியம் ஆக்சைடைத் தருவதற்காக இக்கார்பனேட்டு தளத்திலேயே உருவாக்கப்படுகிறது. இது இரும்பைச் சுத்திகரிப்பதற்கு பெரிதும் உதவுகிறது.
- எண்ணெய் தொழிற்சாலைகளில் துளையிடும் திரவமாக கால்சியம் கார்பனேட்டு பயன்படுத்தப்படுகிறது.
- சர்க்கரை தயாரிப்பில் சர்க்கரையை சுத்திகரிப்பதில் ஒரு மூலப்பொருளாக இது பயன்படுத்தப்படுகிறது. ஆந்த்ரசைட்டுடன் சேர்த்து சூளையில் இட்டு இதை நீற்றுவதன் மூலம் கால்சியம் ஆக்சைடு மற்றும் கார்பன் டை ஆக்சைடு ஆகியவற்றை உற்பத்தி செய்ய முடியும். இவை இச்சுத்திகரிப்பில் பயன்படுகின்றன.
- கால்சியம் கார்பனேட்டு பாரம்பரியமாக கரிம்பலகைச் சுண்ணாம்பின் ஒரு முக்கிய கூறாக இருந்து வருகிறது. இருப்பினும் நவீன உற்பத்தி முறைகள் பெரும்பாலும் கிப்சம் உப்பு, நீரேற்று கால்சியம் சல்பேட் (CaSO4 • 2H2O) ஆகியனவற்றைப் பயன்படுத்துகின்றன.
- நுண் துகளாக உருவாக்கப்படும் கால்சியம் கார்பனேட்டு அணையாடைகளின் ஒரு முக்கிய பகுதிப்பொருள் ஆகும்,
- வண்ணம் மற்றும் சாயத் தொழில், பீங்கான் தொழில் ஆகிய துறைகளிலும் கால்சியம் கார்பனேட்டு பயன்படுத்தப்படுகிறது.
மருத்துவப் பயன்கள்
தொகு- கால்சியம் கார்பனேட்டு மருத்துவ ரீதியாக பரவலாக பயன்படுத்தப்படுகிறது, கால்சியம் சத்தைக் கொடுக்கும் உணவுக் கூட்டுப் பொருளாக இதைப் பயன்படுத்துகிறார்கள். இரைப்பை அமில நீக்கியாகவும், சிறுநீரக பாதிப்பால் இரத்தத்தில் பாசுப்பேட்டு அளவு அதிகரிக்கும்போது சிகிச்சை அளிக்கவும் இதைப் பயன்படுத்துகிறார்கள். மாத்திரைகள் மற்றும் பிற மருந்துகள் ஒரு மந்த நிரப்பியாக மருந்து துறையில் இது பயன்படுத்தப்படுகிறது.
- கால்சியம் ஆக்சைடு மற்றும் பற்பசை தயாரிக்கவும் கால்சியம் கார்பனேட்டு பயன்படுத்தப்படுகிறது. மேலும், நிறம் பராமரிப்பு மற்றும் உணவுப் பாதுகாப்புப் பொருளாகவும் இது பயன்படுத்தப்படுகிறது.
- கால்நடைகள் மற்றும் உயர் கால்சியம் உணவுகளில் இருந்து கிடைக்கும் அதிக கால்சியம் பால்-ஆல்கலி நோய்க்குறியை ஏற்படுத்துகிறது. இது கடுமையான நச்சுத்தன்மையைக் கொண்டிருக்கிறது மற்றும் மரணத்தையும் உண்டாக்குகிறது. இதனால் வாந்தி, வயிற்று வலி, மூளை பாதிப்பு மூலம் மரணம் வரை நிகழ வாய்ப்பு உண்டு.
- ஓர் உணவுக் கூட்டுப் பொருளாக கால்சியம் கார்பனேட்டு அங்கீகரிக்கப்பட்டு ஐரோப்பிய ஒன்றிய எண் 170 என அளிக்கப்பட்டுள்ளது. பசும்பாலில் அதிக அளவு கால்சியம் கார்பனேட்டு உள்ளது என அங்கீகரிக்கப்பட்டுள்ளது. அமெரிக்கா, ஆத்திரேலியா, நியூசிலாந்து முதலிய நாடுகள் இதை அங்கீகரித்துள்ளன.
விவசாயப் பயன்
தொகு- மண்ணின் அமிலத்தன்மையை குறைக்க விவசாய சுண்ணாம்பாக கால்சியம் கார்பனேட்டு பயன்படுத்தப்படுகிறது. இது மண்ணின் pH மதிப்பை உயர்த்துகிறது. pH மதிப்பு குறைவாக இருந்தால் அமிலத்தன்மை அதிகமாக இருக்கும்.
- தாவரங்களுத் தேவையான மக்னீசியம் மற்றும் கால்சியம் உப்புகளுக்கு இது ஆதார மூலமாகத் திகழ்கிறது
- மண்ணின் தண்ணீர் ஊடுறுவும் தன்மையை அதிகரிக்கச் செய்கிறது.
வீடுகளில் துப்புரவுப் பணிக்காக கால்சியம் கார்பனேட்டு பயன்படுத்தப்படுகிறது. சுற்றுச் சூழலில் மண் மற்றும் நீரின் அமிலத்தன்மையை முறைப்படுத்த கால்சியம் கார்பனேட்டு பயன்படுத்தப்படுகிறது. புதை பொருட்களை எரிக்கும்போது அவற்றிலுள்ள SO2 மற்றும் NO2 உமிழ்வுகளைக் குறைப்பதற்காக கால்சியம் கார்பனேட்டு சேர்க்கப்படுகிறது.
மேற்கோள்கள்
தொகு- ↑ "Occupational safety and health guideline for calcium carbonate" (PDF). US Dept. of Health and Human Services. பார்க்கப்பட்ட நாள் 31 March 2011.
- ↑ Aylward, Gordon; Findlay, Tristan (2008). SI Chemical Data Book (4th ed.). John Wiley & Sons Australia, Ltd. பன்னாட்டுத் தரப்புத்தக எண் 978-0-470-81638-7.
- ↑ Rohleder, J.; Kroker, E. (2001). Calcium Carbonate: From the Cretaceous Period Into the 21st Century. Springer Science & Business Media. பன்னாட்டுத் தரப்புத்தக எண் 3-7643-6425-4.
- ↑ Benjamin, Mark M. (2002). Water Chemistry. McGraw-Hill. பன்னாட்டுத் தரப்புத்தக எண் 0-07-238390-9.
- ↑ 5.0 5.1 Zumdahl, Steven S. (2009). Chemical Principles 6th Ed. Houghton Mifflin Company. p. A21. பன்னாட்டுத் தரப்புத்தக எண் 0-618-94690-X.
- ↑ "NIOSH Pocket Guide to Chemical Hazards #0090". National Institute for Occupational Safety and Health (NIOSH).
- ↑ "Precipitated Calcium Carbonate". Archived from the original on 11 சனவரி 2014. பார்க்கப்பட்ட நாள் 11 January 2014.