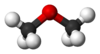
இருமெத்தில் ஈதர்
இருமெத்தில் ஈதர் (Dimethyl ether) என்பது C2H6O அல்லது CH3OCH3 என்ற மூலக்கூற்று வாய்ப்பாடு கொண்ட ஒரு கரிம வேதியியல் சேர்மம் ஆகும். ஆங்கிலத்தில் இச்சேர்மத்தைச் சுருக்கமாக DME என்று அழைப்பார்கள். மெத்தாக்சிமீத்தேன் என்ற வேறொரு பெயராலும் இருமெத்தில் ஈதர் அறியப்படுகிறது. நிறமற்ற வாயுவாகக் காணப்படும் இந்த எளிய ஈதர் மற்ற கரிமச் சேர்மங்கள் தயாரிப்பதற்கான ஒரு முன்னோடியாக விளங்குகிறது. தூசுக்காற்று செலுத்துப்பொருளாகவும் விளங்கும் இச்சேர்மம் எதிர்கால ஆற்றல் வழங்கியாக மாறும் வாய்ப்புடன் ஆராயப்பட்டு வருகிறது. எத்தனாலின் மாற்றீயன் ஆகவும் இருமெத்தில் ஈதர் இருக்கிறது.
| |||
| பெயர்கள் | |||
|---|---|---|---|
| முறையான ஐயூபிஏசி பெயர்
மெத்தாக்சிமீத்தேன்[1] | |||
| வேறு பெயர்கள்
டெமியான்
இருமெத்தில் ஆக்சைடு | |||
| இனங்காட்டிகள் | |||
| 115-10-6 | |||
| Abbreviations | DME | ||
Beilstein Reference
|
1730743 | ||
| ChEBI | CHEBI:28887 | ||
| ChEMBL | ChEMBL119178 | ||
| ChemSpider | 7956 | ||
| EC number | 204-065-8 | ||
| யேமல் -3D படிமங்கள் | Image | ||
| KEGG | C11144 | ||
| ம.பா.த | இருமெத்தில்+ஈதர் | ||
| பப்கெம் | 8254 | ||
| வே.ந.வி.ப எண் | PM4780000 | ||
| |||
| UNII | AM13FS69BX | ||
| UN number | 1033 | ||
| பண்புகள் | |||
| C2H6O | |||
| வாய்ப்பாட்டு எடை | 46.07 g·mol−1 | ||
| தோற்றம் | நிறமற்ற வாயு | ||
| மணம் | குறிப்பிட்ட வகை | ||
| அடர்த்தி | 2.1146 kg/m3 (gas, 0 °C, 1013 mbar)[2] 0.735 g/mL (liquid, -25 °C)[2] | ||
| உருகுநிலை | −141 °C; −222 °F; 132 K | ||
| கொதிநிலை | −24 °C; −11 °F; 249 K | ||
| 71 g dm−3 (at 20 °C (68 °F)) | |||
| மட. P | 0.022 | ||
| ஆவியமுக்கம் | >100 kPa | ||
| இருமுனைத் திருப்புமை (Dipole moment) | 1.30 D | ||
| வெப்பவேதியியல் | |||
| Std enthalpy of formation ΔfH |
−184.1 கியூ மோல்−1 | ||
| Std enthalpy of combustion ΔcH |
−1.4604 MJ mol−1 | ||
| வெப்பக் கொண்மை, C | 65.57 J கி−1 மோல்−1 | ||
| தீங்குகள் | |||
| பொருள் பாதுகாப்பு குறிப்பு தாள் | Oxford MSDS | ||
| GHS pictograms | வார்ப்புரு:GHS சுவாலை | ||
| GHS signal word | அயபாயம் | ||
| H220 | |||
| P210, P410+403 | |||
| ஈயூ வகைப்பாடு | |||
| R-சொற்றொடர்கள் | R12 | ||
| S-சொற்றொடர்கள் | (S2), S9, S16, S33 | ||
| தீப்பற்றும் வெப்பநிலை | −41 °C (−42 °F; 232 K) | ||
Autoignition
temperature |
350 °C (662 °F; 623 K) | ||
| வெடிபொருள் வரம்புகள் | 27% | ||
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |||
தயாரிப்பு
தொகுமெத்தனாலில் இருந்து நீர் நீக்கவினையின் மூலம் 1985 ஆம் ஆண்டில் மட்டும் மேற்கு ஐரோப்பாவில் 50000 டன் இருமெத்தில் ஈதர் தயாரிக்கப்பட்டது:[3]
- 2 CH3OH → (CH3)2O + H2O
இவ்வினைக்குத் தேவையான மெத்தனால் செயற்கை எரிவளியில் இருந்து பெறப்பட்டது. கொள்கைப்படி மெத்தனால் கரிம வேதியியல் கழிவுகளில் இருந்தோ அல்லது உயிர்த்திரளில் இருந்தோ பெறப்பட வேண்டும்[4] . மேலும் சற்று மேம்படுத்தப்பட்ட இரட்டை வினையூக்கித் திட்டங்களில் மெத்தனால் தொகுப்பு மற்றும் நீர்நீக்கம் என்ற இரண்டு செயல்முறைகளும் ஒரே அலகில் மேற்கொள்ளப்படுகிறது. இங்கு மெத்தனாலைத் தனிமைப்படுத்தல், தூய்மைப்படுத்தல் முதலிய செயல்கள் நடைபெறுவதில்லை.
மேற்கண்ட ஒருபடி நிலை உற்பத்தி மற்றும் இரண்டு படிநிலை உற்பத்தி ஆகிய இரண்டு முறைகளும் வர்த்தக நோக்கிலும் பயன்படுகின்றன. நடைமுறையில் இரண்டு படிநிலை தயாரிப்பு முறை பெரிதும் பயந்தருவதாக உள்ளது. எளிமையாகவும் உற்பத்திச் செலவு குறைவாகவும் உள்ளதாகவும் இம்முறை மதிப்பிடப்பட்டுள்ளது.
பயன்கள்
தொகுஇருமெத்தில் சல்பேட்டு என்ற மெத்திலேற்றும் கரணி உற்பத்தி செய்வதற்கு ஊட்ட மூலப்பொருளாக பயன்படுவது இருமெத்தில் ஈதரின் மிகமுக்கியமான பயனாகும். இவ்வினையில் இருமெத்தில் ஈதர், கந்தக மூவாக்சைடுடன் வினைபுரிகிறது.
CH3OCH3 + SO3 → (CH3)2SO4
இப்பயன்பாட்டிற்கு ஒவ்வொரு ஆண்டும் பல ஆயிரக்கணக்கான டன்கள் இருமெத்தில் ஈதர் பயன்படுத்தப்படுகிறது. அசிட்டிக் அமிலத்தை கார்பனைலேற்றத் தொழில் நுட்பத்துடன் தொடர்புடைய மன்சாண்டோ அசிட்டிக்கமிலச் செயல்முறையின் மூலமாகவும் இருமெத்தில் ஈதர் தயாரிக்கப்படுகிறது.
(CH3)2O + 2 CO + H2O → 2 CH3COOH
ஆய்வக வினைப்பொருள் மற்றும் கரைப்பான்
தொகுதாழ் வெப்பநிலை கரைப்பானாகவும் பிரித்தெடுக்கும் வினைப்பொருளாகவும் சில சிறப்பு ஆய்வகச் செயல்முறைகளில் இருமெத்தில் ஈதர் பயன்படுத்தப்படுகிறது. குறைவான கொதிநிலை -23 0 செ வெப்பநிலை இதனுடைய பயன்பாட்டைக் கட்டுபடுத்துகிறது என்றாலும் இதே காரணத்தால், வினைபடும் கலவைகளில் இருந்து இதை எளிதாக பிரித்தெடுக்க முடிகிறது ஆல்க்கைலேற்றும் கரணியான மும்மெத்திலாக்சோனியம் நாற்புளோரோபோரேட்டு தயாரிப்பில் ஒரு முன்னோடியாகவும் இருமெத்தில் ஈதர் செயல்படுகிறது.
தனித்தன்மைப் பயன்பாடுகள்
தொகுஇருமெத்தில் ஈதர் மற்றும் புரோப்பேன் கலவையை உறைய வைத்து பாலுண்ணிகளின் சிகிச்சையில் பயன்படுத்துகிறார்கள்[5]. மின்னணு பொருட்களை சோதிக்கும் உறையவைக்கும் தெளிப்புகளில் இருமெத்தில் ஈதர் முக்கியப் பகுதிப்பொருளாக இருக்கிறது.
எரிபொருள் ஆய்வு
தொகுவீடுகளில் பயன்படுத்தப்படும் திரவ பெட்ரோலியம் வாயுவுக்கு பதிலியாக இருமெத்தில் ஈதர் பயன்படுத்தப்படுகிறது. டீசல் இயந்திரங்களில், பெட்ரோல் பொறிகளில் (30 சதவீதம் இ.மெ.ஈ மற்றும் 70 சதவீதம் தி.பெ.வா மற்றும் வாயுச் சுழலிகளில் எரிபொருளாகப் பயன்படுவதும் இதனுடைய முக்கியப்பயனாகும். டீசல் பொறிகளில் டீசல் எண்ணேயின் சிடேன் எண் 40 முதல் 53 ஆக இருக்கையில் இருமெத்தில் ஈதரின் சிடேன் எண் 55 ஆகவிருப்பது கூடுதல் சிறப்பாகும். டீசல் பொறிகளில் இருமெத்தில் ஈதரை எரிபொருளாகப் பயன்படுத்த பொறியில் மிகச்சிறிய மாறுதலை மட்டுமே செய்ய வேண்டியதாக இருக்கிறது. இந்தக் குறைவு எண்ணிக்கை கார்பன் சேர்மத்தின் இச்சிறப்புப் பண்பு , எரிதலின் போதும் நீடிக்கிறது, அதாவது எரியும்போது இது மிகக்குறைவான NOx, மற்றும் CO வாயுக்களை வெளிவிடுகிறது. கந்தகம் நீங்கிய இவ்வெளிப்பாடு பல்வேறு சர்வதேச அமைப்புகளின் கவனத்தை ஈர்த்திருக்கிறது [6] செயற்கை முறையிலான இரண்டாம் தலைமுறை உயிரி எரிபொருளாக இருமெத்தில் ஈதர் ஐரோப்பிய நாடுகளில் பெரும் வளர்ச்சி அடைந்து வருகிறது 2009 ஆம் ஆண்டில் டென்மார்க் நாட்டின் பல்கலைக்கழக மாணவர்கள் குழு ஒன்று 100 சதவீத இருமெத்தில் ஈதர் எரிபொருளை பயன்படுத்தி ஒரு வாகனத்தை 589 கிலோமீட்டர் தூரம் செலுத்தி பரிசு பெற்றனர். இவர்களின் முந்தைய சாதனை 2007 இல் 306 கிலோமீட்டர் ஆக நிகழ்த்தப்பட்டிருந்தது. என்பது குறிப்பிடத் தகுந்தது.
செயல்முறை
தொகுகீழ்கண்டுள்ள படத்தில் பல்வேறு மூலப்பொருட்களில் இருந்து இருமெத்தில் ஈதரின் தயாரிப்புச் செயல்முறை காட்டப்பட்டுள்ளது.
குளிர்பதனப்பொருள்
தொகுஅமெரிக்க குளிர்பதனப் பொருட்களின் வரையறைகளுக்கு ஏற்புடைய குளிர்பதனப் பொருளாக இருமெத்தில் ஈதர் விளங்குகிறது. அமோனியா, கார்பன் டை ஆக்சைடு, பியூட்டேன் மற்றும் புரோப்பீன் ஆகியவற்றுடன் சேர்த்து உறைபதனக் கலவையாகவும் இதனைப் பயன்படுத்துகிறார்கள்[7] .
பாதுகாப்பு
தொகுஎளிதில் தீப்பற்றக்கூடியதாக இச்சேர்மம் இருந்தாலும் நச்சுத்தன்மை அற்றதாக உள்ளது. மற்ற ஆல்க்கைல் ஈதர்களில் இருந்து மாறுபட்டு தன்னிச்சையான ஆக்சிசனேற்றத்தை தடை செய்கிறது.
மேற்கோள்கள்
தொகு- ↑ "dimethyl ether - PubChem Public Chemical Database". The PubChem Project. USA: National Center for Biotechnology Information.
- ↑ 2.0 2.1 Record in the GESTIS Substance Database of the Institute for Occupational Safety and Health
- ↑ Manfred Müller, Ute Hübsch, “Dimethyl Ether” in Ullmann’s Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim, 2005. எஆசு:10.1002/14356007.a08_541
- ↑ "Dimethyl Ether Technology and Markets 07/08-S3 Report, ChemSystems, December 2008" (PDF). Archived from the original (PDF) on 2009-11-22. பார்க்கப்பட்ட நாள் 2015-08-26.
{{cite web}}: Unknown parameter|=ignored (help) - ↑ IDA Fact Sheet DME/LPG Blends 2010 v1
- ↑ http://www.japantransport.com/conferences/2006/03/dme_detailed_information.pdf பரணிடப்பட்டது 2009-01-07 at the வந்தவழி இயந்திரம், Conference on the Development and Promotion of Environmentally Friendly Heavy Duty Vehicles such as DME Trucks, Washington DC, March 17, 2006
- ↑ http://www.ashrae.org/technology/page/1933#et பரணிடப்பட்டது 2012-01-03 at the வந்தவழி இயந்திரம் ASHRAE list of refrigerants
வெளி இணைப்புகள்
தொகு- The International DME Association
- [1]
- [2] பரணிடப்பட்டது 2015-09-21 at the வந்தவழி இயந்திரம்