சோடியம் தயோசல்பேட்டு
சோடியம் தயோசல்பேட்டு (Sodium thiosulfate) என்பது Na2S2O3 என்ற மூலக்கூற்று வாய்ப்பாட்டால் விவரிக்கப்படும் ஒரு கனிம வேதியியல் சேர்மம் ஆகும். பொதுவாக சோடியம் தயோசல்பேட்டு வெண்மை அல்லது நிறமற்று ஐந்து நீரேற்றாக (Na2S2O3•5H2O) கிடைக்கிறது. திண்மநிலையிலுள்ள சோடியம் தயோசல்பேட்டு நீர் மூலக்கூற்றை இழக்கத் தயாராகவும் தண்ணீரில் நன்றாக கரையக்கூடியதாகவும் உள்ளது.[2] தங்கச் சுரங்கம், நீர் சுத்திகரிப்பு, பகுப்பாய்வு வேதியியல், வெள்ளி அடிப்படையிலான புகைப்பட, திரைப்படத் தொழில் மற்றும் மருத்துவம் ஆகிய துறைகளில் சோடியம் தயோசல்பேட்டு பயன்படுத்தப்படுகிறது. சய்னைடு நச்சு சிகிச்சையிலும் சொறி நோய் எனப்படும் தோல் சிகிச்சையிலும் பயன்படுத்தப்படுவது மருத்துவப் பயன்பாட்டிற்கு உதாரணமாகும்.[3] உலக சுகாதார அமைப்பின் அத்தியாவசிய மருந்துகளின் பட்டியலிலும் சோடியம் தயோசல்பேட்டு இடம்பெற்றுள்ளது.[4][5]

| |
| |

| |
| பெயர்கள் | |
|---|---|
| ஐயூபிஏசி பெயர்
சோடியம் தயோசல்பேட்டு
| |
| வேறு பெயர்கள்
சோடியம் ஐப்போசல்ஃபைட்டு
ஐப்போசல்பைட்டு
| |
| இனங்காட்டிகள் | |
| 7772-98-7 10102-17-7 | |
| ChEBI | CHEBI:132112 |
| ChEMBL | ChEMBL2096650 |
| ChemSpider | 22885 |
| EC number | 231-867-5 |
| யேமல் -3D படிமங்கள் | Image Image |
| பப்கெம் | 24477 |
| வே.ந.வி.ப எண் | XN6476000 |
| |
| UNII | L0IYT1O31N HX1032V43M |
| பண்புகள் | |
| Na2S2O3 | |
| வாய்ப்பாட்டு எடை | 158.11 கி/மோல் (நீரிலி) 248.18 கி/மோல் (ஐந்து நீரேற்று) |
| தோற்றம் | வெண் படிகங்கள் |
| மணம் | நெடியற்றது |
| அடர்த்தி | 1.667 கி/செ.மீ3 |
| உருகுநிலை | 48.3 °C (118.9 °F; 321.4 K) ஐந்து நீரேற்று |
| கொதிநிலை | 100 °C (212 °F; 373 K) ஐந்து நீரேற்று, - 5H2O சிதைவு) |
| 70.1 கி/100 மி.லிட்டர். (20 °செல்சியசு)[1] 231 கி/100 மி.லிட்டர் (100 °செல்சியசு) | |
| கரைதிறன் | ஆல்ககாலில் மிகச் சிறிதளவு கரையும் |
| ஒளிவிலகல் சுட்டெண் (nD) | 1.489 |
| கட்டமைப்பு | |
| படிக அமைப்பு | ஒற்றைச் சாய்வு |
| தீங்குகள் | |
| பொருள் பாதுகாப்பு குறிப்பு தாள் | External MSDS |
| GHS pictograms | 
|
| GHS signal word | எச்சரிக்கை |
| H315, H319, H335 | |
| P261, P264, P271, P280, P302+352, P304+340, P305+351+338, P312, P321, P332+313, P337+313, P362, P403+233, P405 | |
| தீப்பற்றும் வெப்பநிலை | எளிதில் தீப்பற்றாது. |
| தொடர்புடைய சேர்மங்கள் | |
| ஏனைய நேர் மின்அயனிகள் | தயோகந்தக அமிலம் இலித்தியம் தயோசல்பேட்டு பொட்டாசியம் தயோசல்பேட்டு |
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |
பயன்கள்
தொகுசோடியம் தயோசல்பேட்டு முக்கியமாக தொழில்துறையில் பயன்படுத்தப்படுகிறது. உதாரணத்திற்கு சாயங்களை லியூகோ என அழைக்கப்படும் அவற்றின் கரையக்கூடிய நிறமற்ற வடிவங்களுக்கு மாற்ற இது பயன்படுகிறது, கம்பளி, பருத்தி, பட்டு, சோப்புகள், பசைகள், களிமண், மணல், பாக்சைட்டு மற்றும் சமையல் எண்ணெய்கள், உண்ணக்கூடிய கொழுப்புகள் போன்றவற்றை வெளுக்கப் பயன்படுகிறது.[2]
மருத்துவப் பயன்கள்
தொகுசோடியம் தயோசல்பேட்டு சயனைடு நச்சுக்கான சிகிச்சையில் பயன்படுத்தப்படுகிறது.[3] டீனா வெர்சிகோலர் என்ற தோல் நோய்க்கும் தோல் அழற்சி நோய்க்கும் சிகிச்சை அளிக்க சோடியம் தயோ சல்பேட்டு பயன்படுகிறது.[3][6] இரத்தக் கூழ்மப்பகுப்பு,[7] வேதிச்சிகிச்சை[8][9] போன்ற மருத்துவச் செயல்முறைகளிலும் இச்சேர்மம் பயன்படுத்தப்படுகிறது. 2022 ஆம் ஆண்டு செப்டம்பர் மாதத்தில் அமெரிக்க உணவு மற்றும் மருந்து நிர்வாகம் பெட்மார்க் என்ற வர்த்தகப் பெயரில் சோடியம் தயோசல்பேட்டை அங்கீகரித்தது. சிசுப்ளேட்டின் என்ற வேதிச்சிகிச்சை மருந்தைப் பெறும் சிசு, குழந்தைகள் மற்றும் இளம் பருவ புற்றுநோயாளிகளுக்கு காது அல்லது அதன் நரம்பு மண்டலத்தில் நச்சு விளைவைக் கொண்டிருக்கும் காது நோயையும் காது கேளாமையை ஏற்படுத்தும் அபாயத்தையும் இது குறைக்கிறது.[10][11]
புகைப்படத் தொழிலில்
தொகுவெள்ளி புரோமைடு (AgBr) போன்ற வெள்ளி ஆலைடுகள் புகைப்படத் தொழிலில் பயன்படுத்தப்படுகின்றன. புகைப்படங்களை நிலைநிறுத்தும் இப்பயன்பாட்டை சான் எர்சல் என்பவர் கண்டுபிடித்தார். திரைப்படம் மற்றும் புகைப்படங்கள் செயலாக்கத்திற்கு இம்முறை பயன்படுத்தப்படுகிறது. சோடியம் தயோசல்பேட்டு ஒரு புகைப்பட நிலைநிறுத்தி என்று அறியப்படுகிறது. பெரும்பாலும் இது ஐப்போ என்ற பெயரால் குறிப்பிடப்படுகிறது.[12] அம்மோனியம் தயோசல்பேட்டு பொதுவாக சோடியம் தயோசல்பேட்டுக்குப் பதிலாகப் பயன்படுத்தப்படுகிறது.[2]
குளோரினேற்ற தண்ணீரை நடுநிலையாக்குதல்
தொகுமீன்காட்சியகங்கள், நீச்சல் குளங்கள் மற்றும் கனிம நீரூற்றுகளில் பயன்படுத்துவதற்காக குழாய் நீரை குளோரின் நீக்கம் செய்யவும், குளோரின் அளவைக் குறைக்கவும் இது பயன்படுகிறது. நீர் சுத்திகரிப்பு நிலையங்களுக்குள்ளேயே வெளியேறும் நீர் ஆறுகளில் விடுவதற்கு முன் சுத்திகரிக்கவும் இது பயன்படுத்தப்படுகிறது. இந்த குளோரின் ஒடுக்க வினை அயோடின் குறைப்பு வினையை ஒத்த வினையாகும்.[2]
வெளுக்கும் பொருள்களின் காரகாடித்தன்மைச் சுட்டெண் சோதனையில் சோடியம் தயோசல்பேட்டு வெளுக்கும் பொருள்களின் நிறத்தை நீக்கும் விளைவுகளை நடுநிலையாக்குகிறது. வெளுக்கும் கரைசல்களின் காரகாடித்தன்மைச் சுட்டெண்ணை திரவ குறிகாட்டிகளின் உதவியால் சோதிக்க அனுமதிக்கிறது. தொடர்புடைய இவ்வினை அயோடின் வினையை ஒத்ததாகும். வெளுக்கும் பொருள்களில் தீவிரமாகச் செயல்படும் ஐப்போ குளோரைட்டை தயோசல்பேட்டு ஒடுக்குகிறது. அவ்வாறு ஒடுங்கும்போது சல்பேட்டாக ஆக்சிசனேற்றமும் அடைகிறது. இதற்கான முழு வினையின் சமன்பாடு:
- 4 NaClO + Na2S2O3 + 2 NaOH → 4 NaCl + 2 Na2SO4 + H2O
இதேபோல், சோடியம் தயோசல்பேட்டு புரோமினுடன் வினைபுரிந்து, கரைசலில் இருந்து புரோமினை நீக்குகிறது. சோடியம் தயோசல்பேட்டு கரைசல்கள் பொதுவாக வேதியியல் ஆய்வகங்களில் புரோமினுடன் பணிபுரியும் போது முன்னெச்சரிக்கையாகவும், புரோமின், அயோடின் அல்லது பிற வலிமையான ஆக்சிசனேற்றிகளை பாதுகாப்பாக வினையிலிருந்து அகற்றவும் பயன்படுத்தப்படுகின்றன.
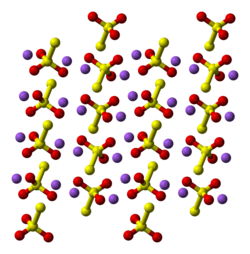
கட்டமைப்பு
தொகுசோடியம் தயோசல்பேட்டின் ஐந்து நீரேற்று இரண்டு பல்லுருவ கட்டமைப்புகளில் காணப்படுகிறது. நீரிலி வடிவம் பல்வேறு பல்லுருவக் கட்டமைப்புகளில் காணப்படுகிறது.[2] திண்ம நிலையில், தாயோசல்பேட்டு அயனி நான்முகி வடிவத்தில் உள்ளது. சல்பேட்டு அயனியில் உள்ள கந்தக அணுவால், ஆக்சிசன் அணுவில் ஒன்று மாற்றப்படுவதால் கருத்தியல் ரீதியாக தாயோசல்பேட்டு அயனி பெறப்படுகிறது. S-S அணுக்களிடையில் காணப்படும் தூரம் ஒற்றைப் பிணைப்பைக் குறிக்கிறது. முனைய கந்தகம் குறிப்பிடத்தக்க எதிர்மறை மின்னூட்டத்தைக் கொண்டுள்ளதையும், S-O அணுக்களிடையேயான இடைவினைகள் அதிக இரட்டைப் பிணைப்புத் தன்மையைக் கொண்டுள்ளன என்பதையும் இது குறிக்கிறது.
தயாரிப்பு
தொகுமுக்கியமாக சோடியம் சல்பைடு தயாரிப்பின் போது வெளியேறும் நீர்மக் கழிவுகள் அல்லது கந்தகச் சாய உற்பத்தியில் கிடைக்கும் கழிவுப் பொருட்களிலிருந்து சோடியம் தயோசல்பேட்டு தொழில்துறை அளவில் தயாரிக்கப்படுகிறது.[13]
சோடியம் சல்பைட்டின் நீரிய கரைசலை கந்தகத்துடன் சேர்த்து சூடாக்கியும் அல்லது நீரிய சோடியம் ஐதராக்சைடுடன் கந்தகத்தைச் சேர்த்து கொதிக்க வைத்தும் இந்த உப்பை ஆய்வக அளவுகளில் தயாரிக்கலாம்::[14][15]
- 6 NaOH + 4 S → 2 Na2S + Na2S2O3 + 3 H2O
வேதிப் பண்புகள்
தொகு300 ° செல்சியசு வெப்பநிலைக்கு சூடாக்கினால் சோடியம் தயோசல்பேட்டு சோடியம் சல்பேட்டு மற்றும் சோடியம் பாலிசல்பைடாக சிதைகிறது:
- 4 Na2S2O3 → 3 Na2SO4 + Na2S5
தயோசல்பேட்டு உப்புகள் அமிலங்களுடன் சேர்த்து சூடுபடுத்தப்படும் போது பண்புரீதியாக சிதைவடைகின்றன. ஆரம்ப புரோட்டானேற்றம் கந்தகத்தில் நிகழ்கிறது. டை எத்தில் ஈதரில் −78 ° செல்சியசில் புரோட்டானேற்றம் நடத்தப்படும்போது, H2S2O3 (தயோசல்பூரிக் அமிலம்) பெறலாம். இது முதல் மற்றும் இரண்டாவது பிரிகைகளில் முறையே 0.6 மற்றும் 1.7 காடித்தன்மை மதிப்பு கொண்ட சற்றே வலுவான அமிலமாகும்.
சாதாரண நிலைமைகளின் கீழ், இந்த உப்பின் அதிகப்படியான கரைசல்களின் அமிலமயமாக்கல், கந்தகம், கந்தக டை ஆக்சைடு மற்றும் தண்ணீராக முழுமையான சிதைவை ஏற்படுத்துகிறது.
- 8 Na2S2O3 + 16 HCl → 16 NaCl + S8 + 8 SO2 + 8 H2O
ஒருங்கிணைப்பு வேதியியல்
தொகுதயோசல்பேட்டு மென்மையான உலோக அயனிகளுக்கு ஒரு சக்திவாய்ந்த ஈந்தணைவியாகும். ஒரு சோடி கந்தக அணுக்கள் பிணைப்பைக் கொண்ட எத்திலீன்டையமீன் ஒரு முக்கியமான தயோசல்பேட்டு ஈந்தணைவியாகும். சோடியம் தயோசல்பேட்டும் அம்மோனியம் தயோசல்பேட்டும் தங்கத்தை பிரித்தெடுப்பதற்காக சயனைடுக்கு மாற்றாக முன்மொழியப்பட்டுள்ளன.[16][2] தயோசல்பேட்டு சயனைடை விட மிகக் குறைவான நச்சுத்தன்மை கொண்டது என்பதும் தங்க சயனைடேற்றத்திற்குப் பொருந்தாத தாது வகைகளை தயோசல்பேட்டால் வெளியேற்ற முடியும் என்பதும் இந்த அணுகுமுறையின் நன்மைகளாகும். இந்த மாற்று செயல்முறையில் சில சிக்கல்களும் உள்ளன. தயோசல்பேட்டின் அதிக நுகர்வும், பொருத்தமான மீட்பு நுட்பம் இல்லாமையும் சில முகியமான சிக்கல்களாகும். ஏனெனில் சோடியம் ஆரோதயோசல்பேட்டு செயல்படுத்தப்பட்ட கார்பனை உறிஞ்சாது. இது தங்க சயனைடேற்றத்தில் தாதுவிலிருந்து தங்கத்தைப் பிரித்தெடுக்க பயன்படுத்தப்படும் நிலையான நுட்பமாகும்.
அயோடின் வெளியேற்ற அளவியல்
தொகுபகுப்பாய்வு வேதியியலில் தயோசல்பேட்டின் மிக முக்கியமான பயன்பாடு வருகிறது. ஏனெனில், தயோசல்பேட்டு அயனியானது அயோடினுடன் விகிதாச்சார முறையில் நீர்த்த கரைசலில் வினைபுரிந்து சோடியம் தயோசல்பேட்டை டெட்ராதயோனேட்டாகவும் அயோடைடாகும் மாற்றுகிறது.
- 2 S2O2−3 + I2 → S4O2−6 + 2 I−
இந்த வினையின் பருமனறி இயல்பு காரணமாகவும், Na2S2O3·5H2O ஒரு சிறந்த நுகர்வுக்கேற்ற கால அளவைக் கொண்டிருப்பதாலும் இது அயோடின் வெளியேற்ற அளவியலில் தரம்பார்க்கப் பயன்படுத்தப்படுகிறது.
தண்ணீரில் கரைந்துள்ள ஆக்சிசனுக்கான விங்கலர் சோதனையில் நீண்ட தொடர் வினைகள் மூலம் நீரின் ஆக்சிசனின் உள்ளடக்கத்தை அளவிட இந்த குறிப்பிட்ட பயன்பாடு அமைகிறது. கரைசலில் கரைந்துள்ள ஐதரசன் பெராக்சைடு போன்ற சில சேர்மங்களின் செறிவுகளை அளவிடுவதிலும், வணிக ரீதியிலான வெளுப்பிகளில் தண்ணீரில் உள்ள குளோரின் உள்ளடக்கத்தை மதிப்பிடுவதிலும் இது பயன்படுத்தப்படுகிறது.
அலுமினிய நேர்மின்னயனி வினை
தொகுசோடியம் தயோசல்பேட்டு பகுப்பாய்வு வேதியியலில் பயன்படுத்தப்படுகிறது.[17] அலுமினிய நேர்மின் அயனி கொண்ட ஒரு மாதிரியுடன் இதை சேர்த்து சூடுபடுத்தினால் வெள்ளை நிற வீழ்படிவு உருவாகும்:
- 2 Al3+ + 3 S2O2−3 + 3 H2O → 3 SO2 + 3 S + 2 Al(OH)3
கரிம வேதியியல்
தொகுசோடியம் தயோசல்பேட்டை அல்கைலேற்றம் செய்தால் கந்தக-அல்கைல்தயோசல்பேட்டுகள் கிடைக்கின்றன. இவை பண்டே உப்புகள் என்று அழைக்கப்படுகின்றன.[18] அல்கைல்தயோசல்பேட்டுகள் நீராற்பகுப்புக்கு ஆளாகின்றன. இதனால் தயோல்கள் கிடைக்கின்றன. இந்த வினை தியோகிளைக்கோலிக் அமிலத்தின் தொகுப்பு வினை மூலம் விளக்கப்படுகிறது:
- ClCH2CO2H + Na2S2O3 → Na[O3S2CH2CO2H] + NaCl
- Na[O3S2CH2CO2H] + H2O → HSCH2CO2H + NaHSO4
மேற்கோள்கள்
தொகு- ↑ Record in the GESTIS Substance Database of the Institute for Occupational Safety and Health
- ↑ 2.0 2.1 2.2 2.3 2.4 2.5 Barbera, J. J.; Metzger, A.; Wolf, M. (2005), "Sulfites, Thiosulfates, and Dithionites", Ullmann's Encyclopedia of Industrial Chemistry, Weinheim: Wiley-VCH, எண்ணிம ஆவணச் சுட்டி:10.1002/14356007.a25_477
{{citation}}: CS1 maint: multiple names: authors list (link) - ↑ 3.0 3.1 3.2 World Health Organization (2009). Stuart MC, Kouimtzi M, Hill SR (eds.). WHO Model Formulary 2008. World Health Organization. pp. 66. hdl:10665/44053. பன்னாட்டுத் தரப்புத்தக எண் 9789241547659.
- ↑ World Health Organization (2019). World Health Organization model list of essential medicines: 21st list 2019. Geneva: World Health Organization. hdl:10665/325771. WHO/MVP/EMP/IAU/2019.06. License: CC BY-NC-SA 3.0 IGO.
- ↑ World Health Organization (2021). World Health Organization model list of essential medicines: 22nd list (2021). Geneva: World Health Organization. hdl:10665/345533. WHO/MHP/HPS/EML/2021.02.
- ↑ "Tinea versicolor". Int. J. Dermatol. 37 (9): 648–55. 2002. doi:10.1046/j.1365-4362.1998.00441.x. பப்மெட்:9762812.
- ↑ "Treatment of Cutaneous Calciphylaxis with Sodium Thiosulfate: Two Case Reports and a Review of the Literature". Am. J. Clin. Dermatol. 12 (5): 339–46. 2011. doi:10.2165/11587060-000000000-00000. பப்மெட்:21834598.
- ↑ "Sodium thiosulfate for prevention of cisplatin-induced hearing loss: updated survival from ACCL0431". The Lancet. Oncology 23 (5): 570–572. May 2022. doi:10.1016/S1470-2045(22)00155-3. பப்மெட்:35489339.
- ↑ "Protection against Cisplatin-Induced Toxicities by N-Acetylcysteine and Sodium Thiosulfate as Assessed at the Molecular, Cellular, and in Vivo Levels". J. Pharmacol. Exp. Ther. 314 (3): 1052–8. 2005. doi:10.1124/jpet.105.087601. பப்மெட்:15951398. https://archive.org/details/sim_journal-of-pharmacology-and-experimental-therapeutics_2005-09_314_3/page/1052.
- ↑ Winstead, Edward (October 6, 2022). "Sodium Thiosulfate Reduces Hearing Loss in Kids with Cancer". National Cancer Institute. பார்க்கப்பட்ட நாள் March 9, 2023.
- ↑ "FDA approves sodium thiosulfate to reduce the risk of ototoxicity associated with cisplatin in pediatric patients with localized, non-metastatic solid tumors". U.S. Food and Drug Administration. 20 September 2022. பார்க்கப்பட்ட நாள் 9 March 2023.
- ↑ Gibson CR (1908). The Romance of Modern Photography, Its Discovery & Its Achievements. Seeley & Co. pp. 37.
hyposulphite-of-soda herschel fixer hypo.
- ↑ Holleman AF, Wiberg E, Wiberg N (2001). Inorganic Chemistry. San Diego: Academic Press. பன்னாட்டுத் தரப்புத்தக எண் 9780123526519.
- ↑ Gordin HM (1913). Elementary Chemistry. Vol. 1. Inorganic Chemistry. Chicago: Medico-Dental Publishing Co. pp. 162 & 287–288.
- ↑ Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ed.). Butterworth–Heinemann. பன்னாட்டுத் தரப்புத்தக எண் 0080379419.
- ↑ "Thiosulfate Leaching of Gold - a Review". Minerals Engineering 14 (2): 135–174. 2001. doi:10.1016/s0892-6875(00)00172-2.
- ↑ Dulski TR (1996). "Ch. 8: Separation by Precypitation". A Manual for the Chemical Analysis of Metals. West Conshohocken, PA: ASTM. p. 99. பன்னாட்டுத் தரப்புத்தக எண் 9781601194350. இணையக் கணினி நூலக மைய எண் 180851384.
- ↑ "Sulfide Synthesis in Preparation of Unsymmetrical Dialkyl Disulfides: Sec-butyl Isopropyl Disulfide". Org. Synth. 58: 147. 1978. doi:10.15227/orgsyn.058.0147. வார்ப்புரு:Free access