காட்மியம் அசிட்டேட்டு
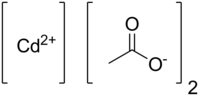
காட்மியம் அசிட்டேட்டு (Cadmium acetate) என்பது Cd(CH3CO2)2 என்ற மூலக்கூற்று வாய்ப்பாடுடன் கூடிய ஒரு வேதிச் சேர்மமாகும்.. நிறமற்ற திடப்பொருளான இச்சேர்மம் ஒரு அணைவுப் பல்லுறுப்பி என்று வகைப்படுத்தப்பட்டுள்ளது. இந்த அணைவுச் சேர்மத்தில் அசிட்டேட்டு ஈனிகள் காட்மியம் உலோக மையங்களுடன் சேர்ந்து இணைந்திருக்கிறது. நீரிலி மற்றும் நீரேற்று என்ற இரண்டு வடிவங்களிலும் இது காணப்படுகிறது. காட்மியம் ஆக்சைடுடன் அசிட்டிக் அமிலத்தைச் சேர்ப்பதன்மூலம் இதைத் தயாரிக்கலாம்:[2][3]
| |
| பெயர்கள் | |
|---|---|
| ஐயூபிஏசி பெயர்
காட்மியம் அசிட்டேட்டு
| |
| வேறு பெயர்கள்
காட்மியம் இருவசிட்டேட்டு
| |
| இனங்காட்டிகள் | |
| 543-90-8 5743-04-4 (dihydrate) | |
| ChemSpider | 10521 |
| EC number | 208-853-2 |
| யேமல் -3D படிமங்கள் | Image |
| பப்கெம் | 10986 |
| வே.ந.வி.ப எண் | AF7505000 |
| |
| பண்புகள் | |
| Cd(CH3COO)2 (நீரிலி) Cd(CH3COO)2·2H2O (இருநீரேற்று) | |
| வாய்ப்பாட்டு எடை | 230.500 கி/மோல் (நீரிலி) 266.529 கி/மோல் (இருநீரேற்று) |
| தோற்றம் | நிறமற்ற படிகங்கள் (நீரிலி) வெண்மைநிற படிகங்கள் (இருநீரேற்று) |
| மணம் | அசிட்டிக் அமிலம் |
| அடர்த்தி | 2.341 g/cm3 (நீரிலி) 2.01 g/cm3 (இருநீரேற்று) |
| உருகுநிலை | 255 °C (491 °F; 528 K) (நீரிலி) இருநீரேற்று 130 பாகை செல்சியசு வெப்பநிலையில் சிதைவடையும் [1] |
| கரையும் (நீரிலி), மிகவும் கரையும் (நீரேற்று) | |
| கரைதிறன் | (நீரிலி) மெத்தனால், எத்தனால் ஆகியன்வற்றில் கரையும் இருநீரேற்று வடிவம்ஏத்தனாலில் கரையும். (இருநீரேற்று) |
| கட்டமைப்பு | |
| படிக அமைப்பு | ஒற்றைச்சரிவு |
| தீங்குகள் | |
| R-சொற்றொடர்கள் | R20/21/22 |
| S-சொற்றொடர்கள் | (S2) S22[2] |
| தொடர்புடைய சேர்மங்கள் | |
| ஏனைய எதிர் மின்னயனிகள் | காட்மியம் புளோரைடு காட்மியம் குளோரைடு காட்மியம் புரோமைடு காட்மியம் அயோடைடு |
| ஏனைய நேர் மின்அயனிகள் | துத்தநாக அசிட்டேட்டு பாதரச(II) அசிட்டேட்டு வெள்ளி அசிட்டேட்டு |
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |
பயன்கள்
தொகுபீங்கான் மற்றும் மண்பாண்டத் தொழிலில் மெருகுப்பூச்சாக காட்மியம் அசிட்டேட்டு பயன்படுகிறது. மின்முலாம் பூசும் தொட்டிகள், நெசவுத் தொழிலில் சாயமூட்டுதல் மற்றும் அச்சிடுதல் ஆகியவற்றில் இது பயனாகிறது. மேலும், கந்தகம், செலினியம், மற்றும் தெல்லூரியம் முதலிய தனிமங்களைப் பகுப்பாய்வு செய்யப் பயன்படும் பகுப்பாய்வு செயலியாகவும் விளங்குகிறது[3].
தயாரிப்பு
தொகுகாட்மியம் ஆக்சைடுடன் அசிட்டிக் அமிலம் சேர்ப்பதன் மூலம் காட்மியம் அசிட்டேட்டைத் தயாரிக்கலாம். இம்முறையைத் தவிர காட்மியம் நைட்ரேட்டுடன் அசிட்டிக் நீரிலியைச் சேர்த்தும் இதைத் தயாரிக்கலாம்.
முன்பாதுகாப்பு
தொகுசர்வதேச புற்றுநோய் ஆய்வு நிறுவனம். காட்மிய சேர்மங்களைத் தொகுதி ஒன்றில் அடங்கியுள்ள புற்றுநோயாக்கிகள் என்று வகைப்படுத்தியுள்ளது.
மேற்கோள்கள்
தொகு- ↑ Lide, David R. (1998). Handbook of Chemistry and Physics (87 ed.). Boca Raton, FL: CRC Press. pp. 447. பன்னாட்டுத் தரப்புத்தக எண் 0-8493-0594-2.
- ↑ 2.0 2.1 Gangolli, S. (1999). The Dictionary of Substances and Their Effects. London: Royal Society of Chemistry. pp. 12–13. பார்க்கப்பட்ட நாள் 2009-03-29.
- ↑ 3.0 3.1 Patnaik, Pradyot (2003). Handbook of Inorganic Chemical Compounds. McGraw-Hill Professional. pp. 143–144. பன்னாட்டுத் தரப்புத்தக எண் 0-07-049439-8. பார்க்கப்பட்ட நாள் 2009-03-29.
| அசிட்டேட்டுகள் | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| AcOH | He | ||||||||||||||||||
| LiOAc | Be(OAc)2 BeAcOH |
B(OAc)3 | AcOAc ROAc |
NH4OAc | AcOOH | FAc | Ne | ||||||||||||
| NaOAc | Mg(OAc)2 | Al(OAc)3 ALSOL Al(OAc)2OH Al2SO4(OAc)4 |
Si | P | S | ClAc | Ar | ||||||||||||
| KOAc | Ca(OAc)2 | Sc(OAc)3 | Ti(OAc)4 | VO(OAc)3 | Cr(OAc)2 Cr(OAc)3 |
Mn(OAc)2 Mn(OAc)3 |
Fe(OAc)2 Fe(OAc)3 |
Co(OAc)2, Co(OAc)3 |
Ni(OAc)2 | Cu(OAc)2 | Zn(OAc)2 | Ga(OAc)3 | Ge | As(OAc)3 | Se | BrAc | Kr | ||
| RbOAc | Sr(OAc)2 | Y(OAc)3 | Zr(OAc)4 | Nb | Mo(OAc)2 | Tc | Ru(OAc)2 Ru(OAc)3 Ru(OAc)4 |
Rh2(OAc)4 | Pd(OAc)2 | AgOAc | Cd(OAc)2 | In | Sn(OAc)2 Sn(OAc)4 |
Sb(OAc)3 | Te | IAc | Xe | ||
| CsOAc | Ba(OAc)2 | Hf | Ta | W | Re | Os | Ir | Pt(OAc)2 | Au | Hg2(OAc)2, Hg(OAc)2 |
TlOAc Tl(OAc)3 |
Pb(OAc)2 Pb(OAc)4 |
Bi(OAc)3 | Po | At | Rn | |||
| Fr | Ra | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |||
| ↓ | |||||||||||||||||||
| La(OAc)3 | Ce(OAc)x | Pr | Nd | Pm | Sm(OAc)3 | Eu(OAc)3 | Gd(OAc)3 | Tb | Dy(OAc)3 | Ho(OAc)3 | Er | Tm | Yb(OAc)3 | Lu(OAc)3 | |||||
| Ac | Th | Pa | UO2(OAc)2 | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | |||||